La quantité maximale d'un soluté dissous dans un solvant à l'équilibre est décrite comme étant la solubilité. Un composé insoluble est un composé qui formera un précipité (un solide cristallin ou amorphe) dans la solution. Il peut être partiellement soluble, mais il est marqué comme insoluble aux fins de la chimie.[1] La mémorisation des règles de solubilité vous facilitera la vie lorsque vous travaillerez avec les équations chimiques. Avec un peu de temps, d'efforts et quelques astuces de mémoire, vous aurez toutes les règles mémorisées en un rien de temps.
Méthode One of Three:
Apprendre les règles de solubilité
-
 1 Reconnaître que les sels contenant des éléments du groupe 1A sont solubles. Le tableau périodique est organisé en lignes et colonnes appelées périodes et groupes, respectivement. La première colonne du tableau contient les éléments du groupe 1A. Ce sont les métaux alcalins et comprennent Li, Na, K, Cs et Rb.[2]
1 Reconnaître que les sels contenant des éléments du groupe 1A sont solubles. Le tableau périodique est organisé en lignes et colonnes appelées périodes et groupes, respectivement. La première colonne du tableau contient les éléments du groupe 1A. Ce sont les métaux alcalins et comprennent Li, Na, K, Cs et Rb.[2] - Par exemple: KCl et LiOH sont solubles dans l'eau.[3]
-
 2 Sachez que les sels contenant des nitrates, des chlorates et des acétates sont solubles. Quand un nitrate, NO3-, chlorate, ClO3-ou acétate, CH3ROUCOULER-, forment un sel, ils sont solubles dans l'eau.[4]
2 Sachez que les sels contenant des nitrates, des chlorates et des acétates sont solubles. Quand un nitrate, NO3-, chlorate, ClO3-ou acétate, CH3ROUCOULER-, forment un sel, ils sont solubles dans l'eau.[4] - Par exemple: KNO3, NaClO3et CH3COONa sont tous solubles.[5]
-
 3 Comprenez que tous les sels d'ammonium sont solubles. L'ion ammonium, NH4+, fait des composés de sel qui se dissocient complètement en présence d'eau. Il n'y a pas d'exceptions à cette règle.[6]
3 Comprenez que tous les sels d'ammonium sont solubles. L'ion ammonium, NH4+, fait des composés de sel qui se dissocient complètement en présence d'eau. Il n'y a pas d'exceptions à cette règle.[6] - Par exemple: NH4OH est soluble même s'il contient un hydroxyde.
-
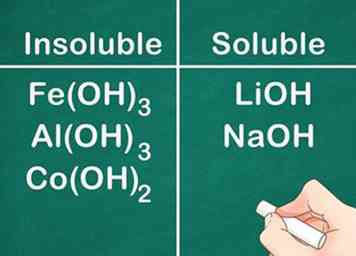 4 Sachez que la plupart des composés hydroxyde sont insolubles. Certains sels d'hydroxyde sont légèrement solubles: des hydroxydes formés avec des éléments du groupe 2 (Ca, Sr et Ba). L'exception à cette règle est que les sels d'hydroxyde formés avec les éléments du groupe 1 sont solubles parce que les éléments du groupe 1A sont toujours solubles.[7]
4 Sachez que la plupart des composés hydroxyde sont insolubles. Certains sels d'hydroxyde sont légèrement solubles: des hydroxydes formés avec des éléments du groupe 2 (Ca, Sr et Ba). L'exception à cette règle est que les sels d'hydroxyde formés avec les éléments du groupe 1 sont solubles parce que les éléments du groupe 1A sont toujours solubles.[7] - Par exemple: Fe (OH)3, Al (OH)3et Co (OH)2 sont insolubles, mais LiOH et NaOH sont solubles.
-
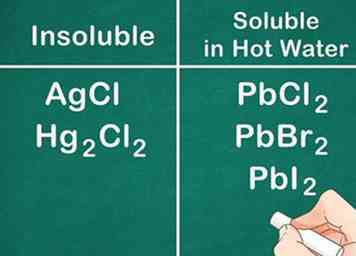 5 Reconnaître que les sels contenant des non-métaux du groupe 17 sont généralement solubles. Les non-métaux du groupe 17 comprennent le chlore (Cl-), le brome (Br-) et de l’iode (I-). Les exceptions à cette règle comprennent l’argent, le plomb et le mercure. Les composés constitués de ces non-métaux et de ces ions, appelés sels d'halogénure, ne sont pas solubles.[8]
5 Reconnaître que les sels contenant des non-métaux du groupe 17 sont généralement solubles. Les non-métaux du groupe 17 comprennent le chlore (Cl-), le brome (Br-) et de l’iode (I-). Les exceptions à cette règle comprennent l’argent, le plomb et le mercure. Les composés constitués de ces non-métaux et de ces ions, appelés sels d'halogénure, ne sont pas solubles.[8] - Par exemple: AgCl et Hg2Cl2 sont tous deux insolubles.
- Notez que PbCl2, PbBr2et PbI2 sont solubles dans l'eau CHAUDE.[9]
-
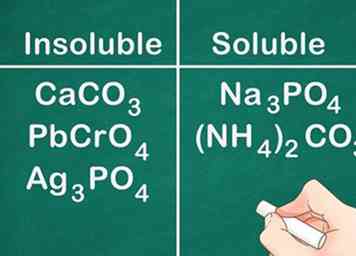 6 Sachez que la plupart des carbonates, chromates et phosphates sont insolubles. Les formules chimiques de chacun de ces éléments sont les suivantes: CO3 (carbonates), CrO4 (chromates) et PO4 (phosphates). Les exceptions à cette règle incluent les métaux du groupe 1A et le NH4+ les composés solubles.
6 Sachez que la plupart des carbonates, chromates et phosphates sont insolubles. Les formules chimiques de chacun de ces éléments sont les suivantes: CO3 (carbonates), CrO4 (chromates) et PO4 (phosphates). Les exceptions à cette règle incluent les métaux du groupe 1A et le NH4+ les composés solubles. - Par exemple: Composés comme CaCO3, PbCrO4et Ag3PO4 sont tous insolubles alors que les composés comme Na3PO4 et (NH4)2CO3 sont solubles.
-
 7 Comprenez que la plupart des sels de sulfate sont solubles. La plupart des composés de sel contenant du SO4 sont solubles dans l'eau. Les exceptions à cette règle incluent les ions suivants Ca+2, Ba+2, Pb+2, Ag+, Sr+2et Hg+2. Les sels de sulfate contenant ces ions sont insolubles.[10]
7 Comprenez que la plupart des sels de sulfate sont solubles. La plupart des composés de sel contenant du SO4 sont solubles dans l'eau. Les exceptions à cette règle incluent les ions suivants Ca+2, Ba+2, Pb+2, Ag+, Sr+2et Hg+2. Les sels de sulfate contenant ces ions sont insolubles.[10] - Par exemple: Na2ALORS4 est complètement soluble, mais CaSO4 et BaSO4 ne sont pas solubles.[11]
-
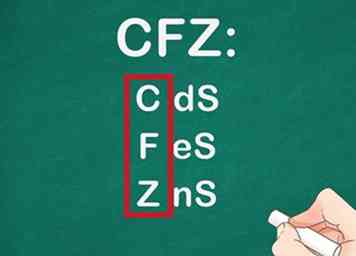
 8 Reconnaître que la plupart des sulfures sont insolubles dans l'eau. Comme pour beaucoup d'autres règles, il existe des exceptions, notamment le baryum, le calcium, le magnésium, le sodium, le potassium et l'ammonium. Seuls les composés sulfurés fabriqués avec ces éléments sont solubles dans l'eau.[12]
8 Reconnaître que la plupart des sulfures sont insolubles dans l'eau. Comme pour beaucoup d'autres règles, il existe des exceptions, notamment le baryum, le calcium, le magnésium, le sodium, le potassium et l'ammonium. Seuls les composés sulfurés fabriqués avec ces éléments sont solubles dans l'eau.[12] - Par exemple: CdS, FeS et ZnS sont tous insolubles.[13]
- Par ailleurs, les sulfures de métaux de transition sont hautement insolubles.
Méthode deux sur trois:
Utilisation du Mnémonique SAG NAG
-
 1 Utilisez le mnémonique NAG SAG. NAG SAG est un moyen facile de mémoriser les composés solubles et les exceptions à la solubilité. Ecrivez SAG NAG comme acrostiche et mémorisez ce que représente chaque lettre.[14] Bien que cette mnémonique n'inclue pas toutes les règles de solubilité, elle en couvre beaucoup. Toutes les lettres représentent des molécules solubles.
1 Utilisez le mnémonique NAG SAG. NAG SAG est un moyen facile de mémoriser les composés solubles et les exceptions à la solubilité. Ecrivez SAG NAG comme acrostiche et mémorisez ce que représente chaque lettre.[14] Bien que cette mnémonique n'inclue pas toutes les règles de solubilité, elle en couvre beaucoup. Toutes les lettres représentent des molécules solubles. - N: Nitrates (NO3-)
- A: Acétate (CH3ROUCOULER-)
- G: métaux alcalins du groupe 1 (Li+, N / a+, etc)
- S: Sulfates (SO4-2)
- A: ions ammonium (NH4+)
- G: Groupe 17 non-métaux (F-, Cl-, Br-, JE-, etc.)
-
 2 Ecrire PMS pour représenter la première exception. P signifie Pb+2 (conduire). M signifie mercure (Hg2+2). S signifie Silver (Ag+). Ces 3 ions ne sont jamais solubles avec le groupe sulfate ou les non-métaux du groupe 17.[15]
2 Ecrire PMS pour représenter la première exception. P signifie Pb+2 (conduire). M signifie mercure (Hg2+2). S signifie Silver (Ag+). Ces 3 ions ne sont jamais solubles avec le groupe sulfate ou les non-métaux du groupe 17.[15] - Lors de l'écriture du mnémonique, placez une étoile à côté du PMS et une étoile similaire à côté du S et du G du SAG pour vous rappeler qu'il s'agit d'exceptions.
-
 3 Rappelez-vous que Castro Bear représente la deuxième exception. Castro Bear peut sembler idiot, mais il représente les 3 ions calcium (Ca+2), Strontium (Sr+2), et le baryum (Ba+2). Ces 3 ions ne sont jamais solubles avec les sulfates.[16]
3 Rappelez-vous que Castro Bear représente la deuxième exception. Castro Bear peut sembler idiot, mais il représente les 3 ions calcium (Ca+2), Strontium (Sr+2), et le baryum (Ba+2). Ces 3 ions ne sont jamais solubles avec les sulfates.[16] - En écrivant le mnémonique, placez une croix à côté de Castro Bear et une autre croix à côté du S dans SAG pour vous rappeler que ces ions font exception à la solubilité du sulfate.
Méthode trois sur trois:
Mémoriser les bases
-
 1 Révisez le matériel fréquemment. Mémoriser n'importe quoi demande du temps et des efforts. Plus vous voyez le matériel fréquemment, plus vous risquez de vous en souvenir plus tard. Lisez les règles souvent et interrogez-vous quotidiennement.
1 Révisez le matériel fréquemment. Mémoriser n'importe quoi demande du temps et des efforts. Plus vous voyez le matériel fréquemment, plus vous risquez de vous en souvenir plus tard. Lisez les règles souvent et interrogez-vous quotidiennement. - Demandez à vos amis et à votre famille de vous interroger sur les règles de solubilité au déjeuner ou au dîner.
- Conservez une copie des règles à portée de main pour vérifier si vous avez des temps d'arrêt.
-
 2 Créez et utilisez des flashcards. Les flashcards sont un excellent moyen de revoir rapidement beaucoup de matériel et de le mémoriser.[17] Créez des fiches contenant les règles de solubilité et des exemples de composés. Parcourez les cartes jusqu'à ce que vous connaissiez les règles et quels composés sont solubles ou non.
2 Créez et utilisez des flashcards. Les flashcards sont un excellent moyen de revoir rapidement beaucoup de matériel et de le mémoriser.[17] Créez des fiches contenant les règles de solubilité et des exemples de composés. Parcourez les cartes jusqu'à ce que vous connaissiez les règles et quels composés sont solubles ou non. - Transportez vos flashcards avec vous et sortez-les si vous êtes assis dans la voiture ou attendez des amis.
- Toute quantité de temps d'arrêt est utile pour examiner les cartes mémoire.
-
 3 Utilisez des mnémoniques. Les mnémoniques sont des astuces de mémoire spéciales qui peuvent vous aider à mémoriser des informations rapidement et facilement.[18] Lors de l'apprentissage d'une mnémonique, il est utile de l'écrire plusieurs fois jusqu'à ce que vous vous en souveniez. Le mnémonique n'est utile que si vous savez ce que tout représente!
3 Utilisez des mnémoniques. Les mnémoniques sont des astuces de mémoire spéciales qui peuvent vous aider à mémoriser des informations rapidement et facilement.[18] Lors de l'apprentissage d'une mnémonique, il est utile de l'écrire plusieurs fois jusqu'à ce que vous vous en souveniez. Le mnémonique n'est utile que si vous savez ce que tout représente! - Pratiquez fréquemment l'écriture du mnémonique et de la signification de chaque lettre pour ne pas oublier.
- Lorsque vous recevez un test ou un quiz, écrivez d'abord le mnémonique pour pouvoir le consulter le reste du temps.
 Minotauromaquia
Minotauromaquia
 1 Reconnaître que les sels contenant des éléments du groupe 1A sont solubles. Le tableau périodique est organisé en lignes et colonnes appelées périodes et groupes, respectivement. La première colonne du tableau contient les éléments du groupe 1A. Ce sont les métaux alcalins et comprennent Li, Na, K, Cs et Rb.[2]
1 Reconnaître que les sels contenant des éléments du groupe 1A sont solubles. Le tableau périodique est organisé en lignes et colonnes appelées périodes et groupes, respectivement. La première colonne du tableau contient les éléments du groupe 1A. Ce sont les métaux alcalins et comprennent Li, Na, K, Cs et Rb.[2]  2 Sachez que les sels contenant des nitrates, des chlorates et des acétates sont solubles. Quand un nitrate, NO3-, chlorate, ClO3-ou acétate, CH3ROUCOULER-, forment un sel, ils sont solubles dans l'eau.[4]
2 Sachez que les sels contenant des nitrates, des chlorates et des acétates sont solubles. Quand un nitrate, NO3-, chlorate, ClO3-ou acétate, CH3ROUCOULER-, forment un sel, ils sont solubles dans l'eau.[4]  3 Comprenez que tous les sels d'ammonium sont solubles. L'ion ammonium, NH4+, fait des composés de sel qui se dissocient complètement en présence d'eau. Il n'y a pas d'exceptions à cette règle.[6]
3 Comprenez que tous les sels d'ammonium sont solubles. L'ion ammonium, NH4+, fait des composés de sel qui se dissocient complètement en présence d'eau. Il n'y a pas d'exceptions à cette règle.[6] 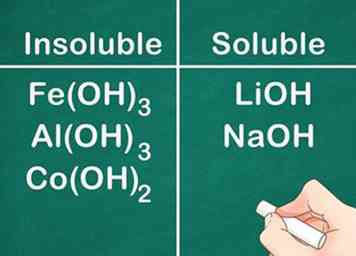 4 Sachez que la plupart des composés hydroxyde sont insolubles. Certains sels d'hydroxyde sont légèrement solubles: des hydroxydes formés avec des éléments du groupe 2 (Ca, Sr et Ba). L'exception à cette règle est que les sels d'hydroxyde formés avec les éléments du groupe 1 sont solubles parce que les éléments du groupe 1A sont toujours solubles.[7]
4 Sachez que la plupart des composés hydroxyde sont insolubles. Certains sels d'hydroxyde sont légèrement solubles: des hydroxydes formés avec des éléments du groupe 2 (Ca, Sr et Ba). L'exception à cette règle est que les sels d'hydroxyde formés avec les éléments du groupe 1 sont solubles parce que les éléments du groupe 1A sont toujours solubles.[7] 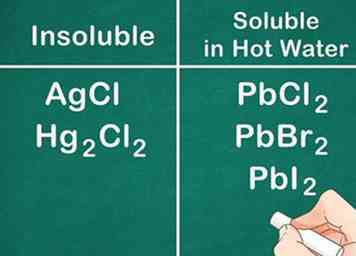 5 Reconnaître que les sels contenant des non-métaux du groupe 17 sont généralement solubles. Les non-métaux du groupe 17 comprennent le chlore (Cl-), le brome (Br-) et de l’iode (I-). Les exceptions à cette règle comprennent l’argent, le plomb et le mercure. Les composés constitués de ces non-métaux et de ces ions, appelés sels d'halogénure, ne sont pas solubles.[8]
5 Reconnaître que les sels contenant des non-métaux du groupe 17 sont généralement solubles. Les non-métaux du groupe 17 comprennent le chlore (Cl-), le brome (Br-) et de l’iode (I-). Les exceptions à cette règle comprennent l’argent, le plomb et le mercure. Les composés constitués de ces non-métaux et de ces ions, appelés sels d'halogénure, ne sont pas solubles.[8] 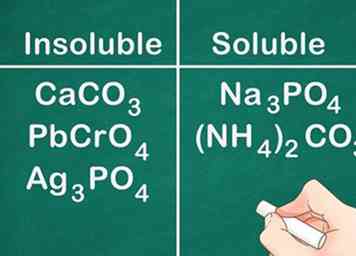 6 Sachez que la plupart des carbonates, chromates et phosphates sont insolubles. Les formules chimiques de chacun de ces éléments sont les suivantes: CO3 (carbonates), CrO4 (chromates) et PO4 (phosphates). Les exceptions à cette règle incluent les métaux du groupe 1A et le NH4+ les composés solubles.
6 Sachez que la plupart des carbonates, chromates et phosphates sont insolubles. Les formules chimiques de chacun de ces éléments sont les suivantes: CO3 (carbonates), CrO4 (chromates) et PO4 (phosphates). Les exceptions à cette règle incluent les métaux du groupe 1A et le NH4+ les composés solubles.  7 Comprenez que la plupart des sels de sulfate sont solubles. La plupart des composés de sel contenant du SO4 sont solubles dans l'eau. Les exceptions à cette règle incluent les ions suivants Ca+2, Ba+2, Pb+2, Ag+, Sr+2et Hg+2. Les sels de sulfate contenant ces ions sont insolubles.[10]
7 Comprenez que la plupart des sels de sulfate sont solubles. La plupart des composés de sel contenant du SO4 sont solubles dans l'eau. Les exceptions à cette règle incluent les ions suivants Ca+2, Ba+2, Pb+2, Ag+, Sr+2et Hg+2. Les sels de sulfate contenant ces ions sont insolubles.[10]  8 Reconnaître que la plupart des sulfures sont insolubles dans l'eau. Comme pour beaucoup d'autres règles, il existe des exceptions, notamment le baryum, le calcium, le magnésium, le sodium, le potassium et l'ammonium. Seuls les composés sulfurés fabriqués avec ces éléments sont solubles dans l'eau.[12]
8 Reconnaître que la plupart des sulfures sont insolubles dans l'eau. Comme pour beaucoup d'autres règles, il existe des exceptions, notamment le baryum, le calcium, le magnésium, le sodium, le potassium et l'ammonium. Seuls les composés sulfurés fabriqués avec ces éléments sont solubles dans l'eau.[12]  1 Utilisez le mnémonique NAG SAG. NAG SAG est un moyen facile de mémoriser les composés solubles et les exceptions à la solubilité. Ecrivez SAG NAG comme acrostiche et mémorisez ce que représente chaque lettre.[14] Bien que cette mnémonique n'inclue pas toutes les règles de solubilité, elle en couvre beaucoup. Toutes les lettres représentent des molécules solubles.
1 Utilisez le mnémonique NAG SAG. NAG SAG est un moyen facile de mémoriser les composés solubles et les exceptions à la solubilité. Ecrivez SAG NAG comme acrostiche et mémorisez ce que représente chaque lettre.[14] Bien que cette mnémonique n'inclue pas toutes les règles de solubilité, elle en couvre beaucoup. Toutes les lettres représentent des molécules solubles.  2 Ecrire PMS pour représenter la première exception. P signifie Pb+2 (conduire). M signifie mercure (Hg2+2). S signifie Silver (Ag+). Ces 3 ions ne sont jamais solubles avec le groupe sulfate ou les non-métaux du groupe 17.[15]
2 Ecrire PMS pour représenter la première exception. P signifie Pb+2 (conduire). M signifie mercure (Hg2+2). S signifie Silver (Ag+). Ces 3 ions ne sont jamais solubles avec le groupe sulfate ou les non-métaux du groupe 17.[15]  3 Rappelez-vous que Castro Bear représente la deuxième exception. Castro Bear peut sembler idiot, mais il représente les 3 ions calcium (Ca+2), Strontium (Sr+2), et le baryum (Ba+2). Ces 3 ions ne sont jamais solubles avec les sulfates.[16]
3 Rappelez-vous que Castro Bear représente la deuxième exception. Castro Bear peut sembler idiot, mais il représente les 3 ions calcium (Ca+2), Strontium (Sr+2), et le baryum (Ba+2). Ces 3 ions ne sont jamais solubles avec les sulfates.[16]  1 Révisez le matériel fréquemment. Mémoriser n'importe quoi demande du temps et des efforts. Plus vous voyez le matériel fréquemment, plus vous risquez de vous en souvenir plus tard. Lisez les règles souvent et interrogez-vous quotidiennement.
1 Révisez le matériel fréquemment. Mémoriser n'importe quoi demande du temps et des efforts. Plus vous voyez le matériel fréquemment, plus vous risquez de vous en souvenir plus tard. Lisez les règles souvent et interrogez-vous quotidiennement.  2 Créez et utilisez des flashcards. Les flashcards sont un excellent moyen de revoir rapidement beaucoup de matériel et de le mémoriser.[17] Créez des fiches contenant les règles de solubilité et des exemples de composés. Parcourez les cartes jusqu'à ce que vous connaissiez les règles et quels composés sont solubles ou non.
2 Créez et utilisez des flashcards. Les flashcards sont un excellent moyen de revoir rapidement beaucoup de matériel et de le mémoriser.[17] Créez des fiches contenant les règles de solubilité et des exemples de composés. Parcourez les cartes jusqu'à ce que vous connaissiez les règles et quels composés sont solubles ou non.  3 Utilisez des mnémoniques. Les mnémoniques sont des astuces de mémoire spéciales qui peuvent vous aider à mémoriser des informations rapidement et facilement.[18] Lors de l'apprentissage d'une mnémonique, il est utile de l'écrire plusieurs fois jusqu'à ce que vous vous en souveniez. Le mnémonique n'est utile que si vous savez ce que tout représente!
3 Utilisez des mnémoniques. Les mnémoniques sont des astuces de mémoire spéciales qui peuvent vous aider à mémoriser des informations rapidement et facilement.[18] Lors de l'apprentissage d'une mnémonique, il est utile de l'écrire plusieurs fois jusqu'à ce que vous vous en souveniez. Le mnémonique n'est utile que si vous savez ce que tout représente!