Bien que vous puissiez augmenter le niveau de l'eau en ajoutant plus de masse (par exemple, plus d'eau ou d'un autre matériau), il existe une expérience commune conçue pour que l'eau «monte» dans un verre. Avec seulement quelques éléments, vous pouvez utiliser les principes de la loi de Charles (qui stipule que la température du gaz est directement proportionnelle au volume du gaz lorsqu'il est sous pression constante) pour impressionner et intriguer un public avec cette expérience.
Méthode One of Three:
Mise en place de l'expérience
-
 1 Remplissez une casserole d'eau. La casserole devrait avoir au moins 1 à 2 pouces (2,5 à 5,1 cm) de profondeur. Vous avez besoin d'une casserole qui puisse contenir suffisamment d'eau pour que tout ne soit pas aspiré dans le verre. Si toute l'eau est aspirée dans le verre, alors de l'air pourra pénétrer. L'eau étant plus lourde que l'air, elle tombera du verre à cause de la gravité.[1]
1 Remplissez une casserole d'eau. La casserole devrait avoir au moins 1 à 2 pouces (2,5 à 5,1 cm) de profondeur. Vous avez besoin d'une casserole qui puisse contenir suffisamment d'eau pour que tout ne soit pas aspiré dans le verre. Si toute l'eau est aspirée dans le verre, alors de l'air pourra pénétrer. L'eau étant plus lourde que l'air, elle tombera du verre à cause de la gravité.[1] -
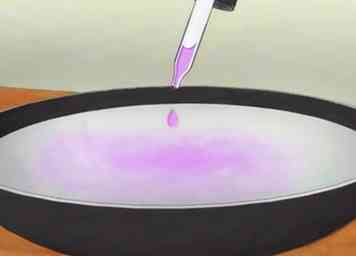 2 Ajoutez du colorant alimentaire à l'eau si désiré. Le colorant alimentaire ne contribue en rien à la science impliquée. Cependant, cela rend l'eau plus facile à voir car elle monte dans le verre. Ceci est particulièrement important pour un large public qui pourrait ne pas être en mesure de se rapprocher du verre.[2]
2 Ajoutez du colorant alimentaire à l'eau si désiré. Le colorant alimentaire ne contribue en rien à la science impliquée. Cependant, cela rend l'eau plus facile à voir car elle monte dans le verre. Ceci est particulièrement important pour un large public qui pourrait ne pas être en mesure de se rapprocher du verre.[2] -
 3 Ramassez tous les autres matériaux nécessaires. Avant de commencer, assurez-vous d’avoir un verre, une bougie et un briquet. Peu importe le type de match ou le briquet que vous utilisez. Vous devez utiliser un verre et non un gobelet en plastique. L'utilisation d'une bougie courte empêche également la flamme de toucher directement le verre. Cependant, la bougie doit être suffisamment haute pour que la mèche ne soit pas mouillée lorsque vous la mettez dans la casserole d'eau.
3 Ramassez tous les autres matériaux nécessaires. Avant de commencer, assurez-vous d’avoir un verre, une bougie et un briquet. Peu importe le type de match ou le briquet que vous utilisez. Vous devez utiliser un verre et non un gobelet en plastique. L'utilisation d'une bougie courte empêche également la flamme de toucher directement le verre. Cependant, la bougie doit être suffisamment haute pour que la mèche ne soit pas mouillée lorsque vous la mettez dans la casserole d'eau. - Si vous essayez de remplacer un verre par un gobelet en plastique, celui-ci fondra et l'expérience échouera.
- Les bougies chauffe-plat fonctionnent bien pour cette expérience.
Méthode deux sur trois:
Faire que l'eau monte dans le verre
-
 1 Mettez la bougie dans la casserole d'eau. Assurez-vous de ne pas mouiller la mèche. Allumez la bougie au centre de la casserole d'eau.[3]
1 Mettez la bougie dans la casserole d'eau. Assurez-vous de ne pas mouiller la mèche. Allumez la bougie au centre de la casserole d'eau.[3] - Si vous utilisez une bougie chauffe-plat, celle-ci sera placée seule dans la casserole. Si vous utilisez une grande bougie mince, il peut se renverser. Pour éviter cela, utilisez un bougeoir court pour stabiliser la bougie.
-
 2 Placez le verre sur la bougie. Retournez le verre à l'envers et placez-le au-dessus de la bougie. Assurez-vous que l'ouverture du verre est complètement immergée dans l'eau. Cela fournit un joint qui empêche l'air d'entrer dans le verre et permet à l'eau de monter dans le verre.[4]
2 Placez le verre sur la bougie. Retournez le verre à l'envers et placez-le au-dessus de la bougie. Assurez-vous que l'ouverture du verre est complètement immergée dans l'eau. Cela fournit un joint qui empêche l'air d'entrer dans le verre et permet à l'eau de monter dans le verre.[4] - Si la bougie touche le verre, vous pouvez soit obtenir une bougie plus courte ou un verre plus grand. Cela garantira que l'expérience se passe bien.
-
 3 Surveillez les bulles. Lorsque la bougie brûle, elle chauffe le gaz à l'intérieur du verre. Cela provoquera l'expansion du gaz, augmentant la pression à l'intérieur du verre. Un peu de gaz devra s'échapper du verre pour soulager la pression. La seule façon pour le gaz de s'échapper est de traverser l'eau au fond du verre. Une fois que la pression est suffisamment élevée, le gaz n'aura d'autre choix que de sortir dans l'eau. [5]
3 Surveillez les bulles. Lorsque la bougie brûle, elle chauffe le gaz à l'intérieur du verre. Cela provoquera l'expansion du gaz, augmentant la pression à l'intérieur du verre. Un peu de gaz devra s'échapper du verre pour soulager la pression. La seule façon pour le gaz de s'échapper est de traverser l'eau au fond du verre. Une fois que la pression est suffisamment élevée, le gaz n'aura d'autre choix que de sortir dans l'eau. [5] -
 4 Laisser la bougie s'éteindre. La bougie allumée convertit 2 molécules d’oxygène (2O2) et 1 molécule de cire de paraffine (CH4) à 1 molécule de dioxyde de carbone (CO2) et 2 molécules d'eau (2H2O). En l'absence d'air dans le verre, la bougie brûlera tout l'oxygène disponible. Lorsque l'oxygène s'épuise, le feu sur la bougie ne peut plus brûler.[6]
4 Laisser la bougie s'éteindre. La bougie allumée convertit 2 molécules d’oxygène (2O2) et 1 molécule de cire de paraffine (CH4) à 1 molécule de dioxyde de carbone (CO2) et 2 molécules d'eau (2H2O). En l'absence d'air dans le verre, la bougie brûlera tout l'oxygène disponible. Lorsque l'oxygène s'épuise, le feu sur la bougie ne peut plus brûler.[6] - Bien qu'il puisse rester de l'oxygène dans le verre, la bougie s'éteindra lorsqu'elle aura épuisé tout l'oxygène suffisamment proche pour alimenter la flamme.
-
 5 Regardez l'eau monter dans le verre. Lorsque la bougie brûle, le gaz restant se refroidit rapidement. Le gaz de refroidissement se contracte (réduit son volume) et crée un vide dans le verre. La pression extérieure forcera l'eau dans le verre pour remplir le vide.[7]
5 Regardez l'eau monter dans le verre. Lorsque la bougie brûle, le gaz restant se refroidit rapidement. Le gaz de refroidissement se contracte (réduit son volume) et crée un vide dans le verre. La pression extérieure forcera l'eau dans le verre pour remplir le vide.[7] - Ce sera plus facile de voir si vous avez choisi de colorer l'eau avec du colorant alimentaire. Gardez à l’esprit que l’eau ne remplira qu’une partie du verre, car il ya encore du gaz piégé dans le verre.
Méthode trois sur trois:
Comprendre pourquoi l'eau monte dans le verre
-
 1 Savoir quelle réaction chimique a lieu. Il y a beaucoup d'explications incorrectes pour cette expérience. Pour comprendre ce qui se passe réellement, vous devez savoir quelle chimie a lieu. La réaction de combustion se produisant est:[8]
1 Savoir quelle réaction chimique a lieu. Il y a beaucoup d'explications incorrectes pour cette expérience. Pour comprendre ce qui se passe réellement, vous devez savoir quelle chimie a lieu. La réaction de combustion se produisant est:[8] - 2O2 + CH4 → Co2 + 2h2O
-
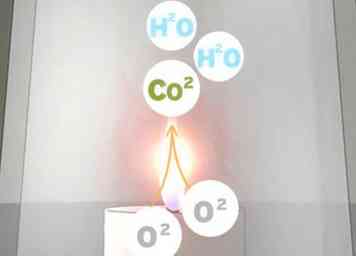 2 Rappelez-vous la loi de Charles. La loi de Charles est une partie de la loi sur les gaz parfaits qui stipule que le volume d'un gaz changera proportionnellement à la température (et vice versa) lorsque la pression extérieure et la masse du gaz resteront constantes. Comme les parois du verre ne modifient pas la pression exercée sur le gaz à l'intérieur, la pression dans cette expérience reste constante. Le gaz ne peut pas pénétrer dans le verre car il est renversé dans l'eau, créant ainsi un sceau.
2 Rappelez-vous la loi de Charles. La loi de Charles est une partie de la loi sur les gaz parfaits qui stipule que le volume d'un gaz changera proportionnellement à la température (et vice versa) lorsque la pression extérieure et la masse du gaz resteront constantes. Comme les parois du verre ne modifient pas la pression exercée sur le gaz à l'intérieur, la pression dans cette expérience reste constante. Le gaz ne peut pas pénétrer dans le verre car il est renversé dans l'eau, créant ainsi un sceau. - Techniquement, puisque la réaction de combustion convertit 2 O2 molécules en 1 CO2 et 2 H2O molécules, la quantité de gaz augmente temporairement. Cependant, la bougie ne maintiendra pas la température à l'intérieur du verre au-dessus de 100 ° C (212 ° F) et le 2H2O molécules vont se condenser en eau liquide. Cela signifie que la quantité de gaz dans le verre diminue efficacement lorsque la bougie brûle.[9]
- La loi de Charles ne s'applique dans ce cas que parce que la quantité de gaz dans le verre reste constante à partir du moment où la bougie brûle. Sans la combustion, plus aucun gaz n'est consommé ou produit. La source de chaleur disparaît simultanément, permettant au gaz de se refroidir et de diminuer en volume.[10]
-
 3 Considérez ce qui se passe lorsque le gaz refroidit. Le volume du gaz étant proportionnel à la température, il diminue à mesure que le gaz refroidit. Cette diminution de volume crée un vide à l'intérieur du verre. La pression à l'extérieur du verre reste la même, ce qui crée un différentiel de pression.[11]
3 Considérez ce qui se passe lorsque le gaz refroidit. Le volume du gaz étant proportionnel à la température, il diminue à mesure que le gaz refroidit. Cette diminution de volume crée un vide à l'intérieur du verre. La pression à l'extérieur du verre reste la même, ce qui crée un différentiel de pression.[11] -
 4 Comprendre les différentiels de pression. Dans un système donné, les fluides passent de l'extrémité haute pression à l'extrémité basse pression. Avec l'air scellé hors du verre, l'eau est forcée de l'extrémité haute pression du système (à l'extérieur du verre) à l'extrémité basse pression du système (à l'intérieur du verre) jusqu'à ce que la pression à l'intérieur du verre soit égale à la pression extérieure le verre.[12]
4 Comprendre les différentiels de pression. Dans un système donné, les fluides passent de l'extrémité haute pression à l'extrémité basse pression. Avec l'air scellé hors du verre, l'eau est forcée de l'extrémité haute pression du système (à l'extérieur du verre) à l'extrémité basse pression du système (à l'intérieur du verre) jusqu'à ce que la pression à l'intérieur du verre soit égale à la pression extérieure le verre.[12] - C'est un peu comme ouvrir un robinet. La pression à l'extérieur de la conduite d'eau est inférieure à la pression à l'intérieur de la conduite, de sorte que l'eau est forcée de traverser la canalisation et de sortir du robinet (même si cela doit aller à l'encontre de la gravité).
Facebook
Twitter
Google+
 Minotauromaquia
Minotauromaquia
 1 Remplissez une casserole d'eau. La casserole devrait avoir au moins 1 à 2 pouces (2,5 à 5,1 cm) de profondeur. Vous avez besoin d'une casserole qui puisse contenir suffisamment d'eau pour que tout ne soit pas aspiré dans le verre. Si toute l'eau est aspirée dans le verre, alors de l'air pourra pénétrer. L'eau étant plus lourde que l'air, elle tombera du verre à cause de la gravité.[1]
1 Remplissez une casserole d'eau. La casserole devrait avoir au moins 1 à 2 pouces (2,5 à 5,1 cm) de profondeur. Vous avez besoin d'une casserole qui puisse contenir suffisamment d'eau pour que tout ne soit pas aspiré dans le verre. Si toute l'eau est aspirée dans le verre, alors de l'air pourra pénétrer. L'eau étant plus lourde que l'air, elle tombera du verre à cause de la gravité.[1]  2 Ajoutez du colorant alimentaire à l'eau si désiré. Le colorant alimentaire ne contribue en rien à la science impliquée. Cependant, cela rend l'eau plus facile à voir car elle monte dans le verre. Ceci est particulièrement important pour un large public qui pourrait ne pas être en mesure de se rapprocher du verre.[2]
2 Ajoutez du colorant alimentaire à l'eau si désiré. Le colorant alimentaire ne contribue en rien à la science impliquée. Cependant, cela rend l'eau plus facile à voir car elle monte dans le verre. Ceci est particulièrement important pour un large public qui pourrait ne pas être en mesure de se rapprocher du verre.[2]  3 Ramassez tous les autres matériaux nécessaires. Avant de commencer, assurez-vous d’avoir un verre, une bougie et un briquet. Peu importe le type de match ou le briquet que vous utilisez. Vous devez utiliser un verre et non un gobelet en plastique. L'utilisation d'une bougie courte empêche également la flamme de toucher directement le verre. Cependant, la bougie doit être suffisamment haute pour que la mèche ne soit pas mouillée lorsque vous la mettez dans la casserole d'eau.
3 Ramassez tous les autres matériaux nécessaires. Avant de commencer, assurez-vous d’avoir un verre, une bougie et un briquet. Peu importe le type de match ou le briquet que vous utilisez. Vous devez utiliser un verre et non un gobelet en plastique. L'utilisation d'une bougie courte empêche également la flamme de toucher directement le verre. Cependant, la bougie doit être suffisamment haute pour que la mèche ne soit pas mouillée lorsque vous la mettez dans la casserole d'eau.  1 Mettez la bougie dans la casserole d'eau. Assurez-vous de ne pas mouiller la mèche. Allumez la bougie au centre de la casserole d'eau.[3]
1 Mettez la bougie dans la casserole d'eau. Assurez-vous de ne pas mouiller la mèche. Allumez la bougie au centre de la casserole d'eau.[3]  2 Placez le verre sur la bougie. Retournez le verre à l'envers et placez-le au-dessus de la bougie. Assurez-vous que l'ouverture du verre est complètement immergée dans l'eau. Cela fournit un joint qui empêche l'air d'entrer dans le verre et permet à l'eau de monter dans le verre.[4]
2 Placez le verre sur la bougie. Retournez le verre à l'envers et placez-le au-dessus de la bougie. Assurez-vous que l'ouverture du verre est complètement immergée dans l'eau. Cela fournit un joint qui empêche l'air d'entrer dans le verre et permet à l'eau de monter dans le verre.[4]  3 Surveillez les bulles. Lorsque la bougie brûle, elle chauffe le gaz à l'intérieur du verre. Cela provoquera l'expansion du gaz, augmentant la pression à l'intérieur du verre. Un peu de gaz devra s'échapper du verre pour soulager la pression. La seule façon pour le gaz de s'échapper est de traverser l'eau au fond du verre. Une fois que la pression est suffisamment élevée, le gaz n'aura d'autre choix que de sortir dans l'eau. [5]
3 Surveillez les bulles. Lorsque la bougie brûle, elle chauffe le gaz à l'intérieur du verre. Cela provoquera l'expansion du gaz, augmentant la pression à l'intérieur du verre. Un peu de gaz devra s'échapper du verre pour soulager la pression. La seule façon pour le gaz de s'échapper est de traverser l'eau au fond du verre. Une fois que la pression est suffisamment élevée, le gaz n'aura d'autre choix que de sortir dans l'eau. [5]  4 Laisser la bougie s'éteindre. La bougie allumée convertit 2 molécules d’oxygène (2O2) et 1 molécule de cire de paraffine (CH4) à 1 molécule de dioxyde de carbone (CO2) et 2 molécules d'eau (2H2O). En l'absence d'air dans le verre, la bougie brûlera tout l'oxygène disponible. Lorsque l'oxygène s'épuise, le feu sur la bougie ne peut plus brûler.[6]
4 Laisser la bougie s'éteindre. La bougie allumée convertit 2 molécules d’oxygène (2O2) et 1 molécule de cire de paraffine (CH4) à 1 molécule de dioxyde de carbone (CO2) et 2 molécules d'eau (2H2O). En l'absence d'air dans le verre, la bougie brûlera tout l'oxygène disponible. Lorsque l'oxygène s'épuise, le feu sur la bougie ne peut plus brûler.[6]  5 Regardez l'eau monter dans le verre. Lorsque la bougie brûle, le gaz restant se refroidit rapidement. Le gaz de refroidissement se contracte (réduit son volume) et crée un vide dans le verre. La pression extérieure forcera l'eau dans le verre pour remplir le vide.[7]
5 Regardez l'eau monter dans le verre. Lorsque la bougie brûle, le gaz restant se refroidit rapidement. Le gaz de refroidissement se contracte (réduit son volume) et crée un vide dans le verre. La pression extérieure forcera l'eau dans le verre pour remplir le vide.[7]  1 Savoir quelle réaction chimique a lieu. Il y a beaucoup d'explications incorrectes pour cette expérience. Pour comprendre ce qui se passe réellement, vous devez savoir quelle chimie a lieu. La réaction de combustion se produisant est:[8]
1 Savoir quelle réaction chimique a lieu. Il y a beaucoup d'explications incorrectes pour cette expérience. Pour comprendre ce qui se passe réellement, vous devez savoir quelle chimie a lieu. La réaction de combustion se produisant est:[8]  2 Rappelez-vous la loi de Charles. La loi de Charles est une partie de la loi sur les gaz parfaits qui stipule que le volume d'un gaz changera proportionnellement à la température (et vice versa) lorsque la pression extérieure et la masse du gaz resteront constantes. Comme les parois du verre ne modifient pas la pression exercée sur le gaz à l'intérieur, la pression dans cette expérience reste constante. Le gaz ne peut pas pénétrer dans le verre car il est renversé dans l'eau, créant ainsi un sceau.
2 Rappelez-vous la loi de Charles. La loi de Charles est une partie de la loi sur les gaz parfaits qui stipule que le volume d'un gaz changera proportionnellement à la température (et vice versa) lorsque la pression extérieure et la masse du gaz resteront constantes. Comme les parois du verre ne modifient pas la pression exercée sur le gaz à l'intérieur, la pression dans cette expérience reste constante. Le gaz ne peut pas pénétrer dans le verre car il est renversé dans l'eau, créant ainsi un sceau.  3 Considérez ce qui se passe lorsque le gaz refroidit. Le volume du gaz étant proportionnel à la température, il diminue à mesure que le gaz refroidit. Cette diminution de volume crée un vide à l'intérieur du verre. La pression à l'extérieur du verre reste la même, ce qui crée un différentiel de pression.[11]
3 Considérez ce qui se passe lorsque le gaz refroidit. Le volume du gaz étant proportionnel à la température, il diminue à mesure que le gaz refroidit. Cette diminution de volume crée un vide à l'intérieur du verre. La pression à l'extérieur du verre reste la même, ce qui crée un différentiel de pression.[11]  4 Comprendre les différentiels de pression. Dans un système donné, les fluides passent de l'extrémité haute pression à l'extrémité basse pression. Avec l'air scellé hors du verre, l'eau est forcée de l'extrémité haute pression du système (à l'extérieur du verre) à l'extrémité basse pression du système (à l'intérieur du verre) jusqu'à ce que la pression à l'intérieur du verre soit égale à la pression extérieure le verre.[12]
4 Comprendre les différentiels de pression. Dans un système donné, les fluides passent de l'extrémité haute pression à l'extrémité basse pression. Avec l'air scellé hors du verre, l'eau est forcée de l'extrémité haute pression du système (à l'extérieur du verre) à l'extrémité basse pression du système (à l'intérieur du verre) jusqu'à ce que la pression à l'intérieur du verre soit égale à la pression extérieure le verre.[12]