La chimie organique est l'étude du carbone et de ses composés chimiques. Le sujet peut être vaste et difficile à comprendre au début. Heureusement, avec persistance, c'est compréhensible. Comprendre la chimie organique est crucial pour quiconque s'intéresse aux produits chimiques naturels ou artificiels, y compris ceux contenus dans les aliments, les boissons et même notre propre corps.
Première partie de trois:
Reconnaître les réactions de chimie organique communes
-
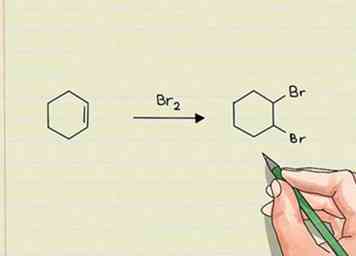 1 Recherchez un nombre accru de liaisons sigma pour identifier les réactions d'addition. En d'autres termes, recherchez un plus grand nombre d'atomes que dans la molécule d'origine. Cela se produit généralement en brisant une liaison pi ou en se liant à un ensemble d'électrons non appariés dans la molécule. Les réactions d'addition ne «transforment» pas un atome ou un groupe en un autre. Ils ajoutent simplement quelque chose de nouveau.[1]
1 Recherchez un nombre accru de liaisons sigma pour identifier les réactions d'addition. En d'autres termes, recherchez un plus grand nombre d'atomes que dans la molécule d'origine. Cela se produit généralement en brisant une liaison pi ou en se liant à un ensemble d'électrons non appariés dans la molécule. Les réactions d'addition ne «transforment» pas un atome ou un groupe en un autre. Ils ajoutent simplement quelque chose de nouveau.[1] - Les réactions d'addition se produisent généralement lorsque des liaisons doubles ou triples sont attaquées. Par exemple, si une double liaison est présente entre deux atomes de carbone et si de l'hydrogène était ajouté à travers la liaison, de l'hydrogène serait ajouté à la molécule. Aucune autre espèce ne partirait.
-
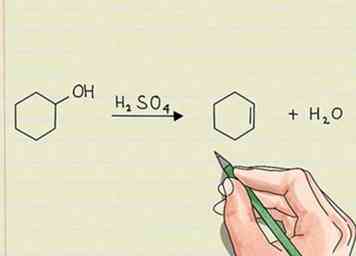 2 Recherchez un nombre accru de liaisons pi pour indiquer les réactions d'élimination. C'est le contraire d'une réaction d'addition. Quelque chose sera retiré de la molécule d'origine et laissera des électrons. Ces électrons non liés se présenteront sous la forme d'une paire isolée ou formeront une liaison pi dans la molécule.[2]
2 Recherchez un nombre accru de liaisons pi pour indiquer les réactions d'élimination. C'est le contraire d'une réaction d'addition. Quelque chose sera retiré de la molécule d'origine et laissera des électrons. Ces électrons non liés se présenteront sous la forme d'une paire isolée ou formeront une liaison pi dans la molécule.[2] - Si vous retirez l'hydrogène d'une chaîne hydrocarbonée, le résultat serait que les électrons non appariés entrent dans une double liaison entre deux des atomes de carbone. Cela ne nécessite rien d'autre à ajouter, il ne supprime que l'hydrogène.
-
 3 Notez tout «échange» moléculaire pour isoler les réactions de substitution. Une réaction de substitution se produit lorsqu'un groupe (A) de la molécule est retiré et remplacé par un nouveau groupe (B). Cela ne change pas nécessairement le nombre de liaisons pi ou sigma dans la molécule, comme vous le verrez avec les réactions d’addition et d’élimination. Les types courants de réactions de substitution sont les suivants:[3]
3 Notez tout «échange» moléculaire pour isoler les réactions de substitution. Une réaction de substitution se produit lorsqu'un groupe (A) de la molécule est retiré et remplacé par un nouveau groupe (B). Cela ne change pas nécessairement le nombre de liaisons pi ou sigma dans la molécule, comme vous le verrez avec les réactions d’addition et d’élimination. Les types courants de réactions de substitution sont les suivants:[3] - Substitution nucléophile - Quand un nucléophile remplace un autre nucléophile dans la réaction.
- Substitution électrophile - Quand un électrophile remplace un autre électrophile dans la réaction.
- SN1 - Une réaction de substitution impliquant une seule molécule dans l'état de transition. En d'autres termes, le groupe partant part en premier, puis le nouveau groupe est libre d'attaquer la molécule.[4]
- SN2 - Dans ce type de réaction, l'état de transition est formé de deux molécules. Cela se produit parce que le nouveau groupe attaque la molécule sur un site disponible et que le groupe partant est forcé de se détacher.[5]
-
 4 Réactions de réarrangement ponctuel lorsque le produit a la même formule que la molécule d'origine. Les réarrangements forment des isomères - des molécules qui ont exactement les mêmes atomes mais dans une configuration différente. Les isomères auront la même formule chimique, mais des propriétés différentes qui sont uniques à leur configuration. Le nombre de liaisons n'est généralement pas affecté dans les réarrangements.[6]
4 Réactions de réarrangement ponctuel lorsque le produit a la même formule que la molécule d'origine. Les réarrangements forment des isomères - des molécules qui ont exactement les mêmes atomes mais dans une configuration différente. Les isomères auront la même formule chimique, mais des propriétés différentes qui sont uniques à leur configuration. Le nombre de liaisons n'est généralement pas affecté dans les réarrangements.[6] - Il existe un sous-ensemble de réactions de réarrangement appelées tautomérisation. C'est à ce moment que deux isomères se déplacent rapidement entre eux.
-
 5 Considérer d'autres réactions importantes qui peuvent affecter les molécules organiques. Les réactions d'oxydo-réduction (ou rédox) sont très courantes en chimie organique, de même que les réactions radicalaires. Vous devriez être un peu familier avec ces réactions de la chimie inorganique générale, mais c'est une bonne idée de les revoir.[7]
5 Considérer d'autres réactions importantes qui peuvent affecter les molécules organiques. Les réactions d'oxydo-réduction (ou rédox) sont très courantes en chimie organique, de même que les réactions radicalaires. Vous devriez être un peu familier avec ces réactions de la chimie inorganique générale, mais c'est une bonne idée de les revoir.[7] - Si vous poursuivez votre quête de la chimie organique, vous rencontrerez des réactions plus complexes qui se produiront dans des conditions spécialisées, mais elles suivront les mêmes bases que toutes les réactions organiques.
Deuxième partie de trois:
Comprendre les tendances de base en chimie organique
-
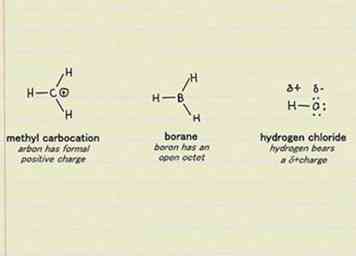 1 Identifier les électrophiles dans les mécanismes de réaction de la chimie organique. Le mot électrophile fait référence aux espèces «aimantes des électrons». Ceci s'applique aux atomes, aux molécules et aux ions. S'il peut accepter une paire d'électrons, il est considéré comme un électrophile. N'oubliez pas que tous les électrophiles n'attirent pas les électrons avec la même intensité. Les électrophiles ayant des électronégativités plus élevées attireront mieux les électrons que ceux ayant des électronégativités plus faibles.[8]
1 Identifier les électrophiles dans les mécanismes de réaction de la chimie organique. Le mot électrophile fait référence aux espèces «aimantes des électrons». Ceci s'applique aux atomes, aux molécules et aux ions. S'il peut accepter une paire d'électrons, il est considéré comme un électrophile. N'oubliez pas que tous les électrophiles n'attirent pas les électrons avec la même intensité. Les électrophiles ayant des électronégativités plus élevées attireront mieux les électrons que ceux ayant des électronégativités plus faibles.[8] - Les cations sont de bons exemples d'électrophiles. Comme ils ont une charge nette positive, ils sont attirés par la charge négative d'un électron. Les halogènes (chlore, fluor, etc.) sont également des électrophiles puissants, car l'acquisition d'un électron remplira leur couche d'électrons la plus externe, ce qui les rendra globalement plus stables.
-
 2 Identifier les nucléophiles dans les mécanismes de réaction de la chimie organique. Les nucléophiles sont le complément parfait aux électrophiles. Un nucléophile est une espèce capable de donner une paire d'électrons. Les espèces ayant des électronégativités plus faibles seront plus en mesure de donner des électrons, ce qui les rendra de meilleurs nucléophiles que les espèces ayant des électronégativités plus élevées.[9]
2 Identifier les nucléophiles dans les mécanismes de réaction de la chimie organique. Les nucléophiles sont le complément parfait aux électrophiles. Un nucléophile est une espèce capable de donner une paire d'électrons. Les espèces ayant des électronégativités plus faibles seront plus en mesure de donner des électrons, ce qui les rendra de meilleurs nucléophiles que les espèces ayant des électronégativités plus élevées.[9] - Les anions ont une charge globale négative et sont souvent capables d'abandonner des électrons pour devenir plus stables. Cela se produit généralement par liaison ionique. Les métaux alcalino-terreux tels que le sodium ont également tendance à être de nature nucléophile, car la libération d'un électron stabilise sa couche d'électrons la plus externe.
-
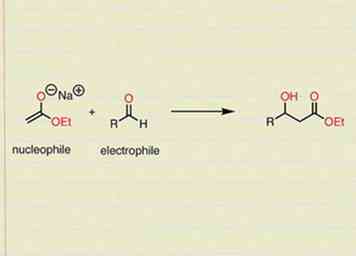 3 Rappelez-vous que les nucléophiles attaquent les électrophiles dans les réactions organiques. Il s’agit, en substance, d’un moyen de considérer les mécanismes de manière cohérente. Vous devriez lire votre mécanisme comme si le composé nucléophile cherche et réagit avec le composé électrophile. Cela vous aidera à vous rappeler par où commencer et où vont les électrons.
3 Rappelez-vous que les nucléophiles attaquent les électrophiles dans les réactions organiques. Il s’agit, en substance, d’un moyen de considérer les mécanismes de manière cohérente. Vous devriez lire votre mécanisme comme si le composé nucléophile cherche et réagit avec le composé électrophile. Cela vous aidera à vous rappeler par où commencer et où vont les électrons. - Un exemple de ceci pourrait être que vous avez une molécule contenant une double liaison entre deux de ses carbones (les électrons pi sont généralement capables de former une autre liaison avec une nouvelle espèce) et une molécule de brome (halogène) attaque cette double liaison.Le résultat serait que la double liaison serait rompue et que le brome serait ajouté à l'un des deux carbones (lequel carbone dépend des conditions et du type de réaction).
-
 4 Familiarisez-vous avec d'autres bases de la chimie organique. Bien que la chimie organique soit un sujet important, il existe d’importants principes sous-jacents qui régissent les réactions plus complexes. Si vous vous familiarisez avec ces principes et que vous comprenez leurs applications, vous serez en mesure de voir comment ils se déroulent dans l’ensemble le plus complexe de réactions organiques. Les fondations les plus importantes sont:[10]
4 Familiarisez-vous avec d'autres bases de la chimie organique. Bien que la chimie organique soit un sujet important, il existe d’importants principes sous-jacents qui régissent les réactions plus complexes. Si vous vous familiarisez avec ces principes et que vous comprenez leurs applications, vous serez en mesure de voir comment ils se déroulent dans l’ensemble le plus complexe de réactions organiques. Les fondations les plus importantes sont:[10] - Stéréochimie - Cela se rapporte à la manière dont la forme et la taille d'une molécule affectent sa réactivité.[11]
- Résonance - C'est quand une molécule a différentes configurations possibles d'électrons. Par exemple, une paire d'électrons pourrait être trouvée dans une double liaison ou sur un groupe fonctionnel proche. Cette flexibilité permet une stabilisation de la molécule.[12]
- Aromatisation - Cela prend la délocalisation des électrons en résonance (la capacité des électrons à être partagés à travers la molécule) à un niveau différent. Dans une molécule aromatique, il y a toujours des électrons pi (4n + 2) et ils sont délocalisés à travers un système de liaison pi conjugué ou dans un cycle (tel que le benzène).[13]
- Groupes fonctionnels - Ces groupes d'atomes sont responsables des différentes caractéristiques des molécules auxquelles ils sont attachés.
Troisième partie de trois:
Etudier efficacement les matériaux de chimie organique
-
 1 Lisez le livre avant de venir en classe. Cela vous permettra de prévisualiser les informations qui seront couvertes dans les conférences. Vous devriez prendre des notes sur ce que vous lisez et assurez-vous qu'elles correspondent aux notes que vous prenez pendant la conférence. Vous devriez également écrire toutes les questions que vous avez pendant la lecture et leur demander si la conférence ne leur répond pas.
1 Lisez le livre avant de venir en classe. Cela vous permettra de prévisualiser les informations qui seront couvertes dans les conférences. Vous devriez prendre des notes sur ce que vous lisez et assurez-vous qu'elles correspondent aux notes que vous prenez pendant la conférence. Vous devriez également écrire toutes les questions que vous avez pendant la lecture et leur demander si la conférence ne leur répond pas. -
 2 Faites des fiches pour différentes réactions organiques. Vous bénéficierez grandement en divisant les grandes quantités d’informations couvertes dans une classe de chimie organique par des fiches. Le système que vous utilisez pour vos notecards dépendra des informations que vous souhaitez apprendre à ce moment-là. Ne jetez pas vos cartes de correspondance. Gardez-les à revoir chaque semaine, et vous serez beaucoup mieux pour l'examen final.[14]
2 Faites des fiches pour différentes réactions organiques. Vous bénéficierez grandement en divisant les grandes quantités d’informations couvertes dans une classe de chimie organique par des fiches. Le système que vous utilisez pour vos notecards dépendra des informations que vous souhaitez apprendre à ce moment-là. Ne jetez pas vos cartes de correspondance. Gardez-les à revoir chaque semaine, et vous serez beaucoup mieux pour l'examen final.[14] - Par exemple, vous pouvez créer un jeu de fiches pour une série de réactions d’ajout que vous étudiez. De même, vous pouvez créer un jeu de fiches couvrant les différents types de réactions (ajout, élimination, substitution, etc.). Vous pouvez créer plusieurs jeux de cartes, tels que les deux mentionnés, qui organisent les informations de différentes manières.
-
 3 Étudier la chimie organique tous les jours du semestre. Les recherches démontrent que l’incorporation de toutes vos études dans une seule et même session n’est pas très efficace. Vous apprendrez beaucoup plus si vous répartissez votre temps d'étude. N'oubliez pas de prendre une pause d'étude toutes les quarante-cinq minutes pour reposer votre cerveau.[15]
3 Étudier la chimie organique tous les jours du semestre. Les recherches démontrent que l’incorporation de toutes vos études dans une seule et même session n’est pas très efficace. Vous apprendrez beaucoup plus si vous répartissez votre temps d'étude. N'oubliez pas de prendre une pause d'étude toutes les quarante-cinq minutes pour reposer votre cerveau.[15] - Assurez-vous de revenir en arrière et de passer en revue le matériel passé chaque semaine. Cela gardera le matériel frais, et peut être fait facilement en examinant vos notecards.
-
 4 Passez du temps à étudier en groupe. Même si vous préférez étudier seul, vous découvrirez différentes manières d’examiner les réactions organiques. D'autres étudiants pourraient être efficaces pour déterminer quelles réactions sont SN1 ou SN2, alors que vous êtes mieux en mesure d'identifier les nucléophiles et les électrophiles. Cet échange de connaissances profitera à tous.[16]
4 Passez du temps à étudier en groupe. Même si vous préférez étudier seul, vous découvrirez différentes manières d’examiner les réactions organiques. D'autres étudiants pourraient être efficaces pour déterminer quelles réactions sont SN1 ou SN2, alors que vous êtes mieux en mesure d'identifier les nucléophiles et les électrophiles. Cet échange de connaissances profitera à tous.[16] - Une autre façon d’appréhender l’apprentissage social consiste à donner des cours à une autre personne ou à trouver un tuteur vous-même.
-
 5 Prenez au sérieux les problèmes de pratique. Travailler à travers des problèmes de pratique forcera votre cerveau à se rappeler les informations que vous avez apprises. C'est une compétence essentielle pour passer le test. C'est aussi une bonne idée de vous chronométrer afin de pouvoir accélérer les problèmes de travail. Essayez de passer des tests d’entraînement et de les terminer dans le même temps que vous aurez en classe.[17]
5 Prenez au sérieux les problèmes de pratique. Travailler à travers des problèmes de pratique forcera votre cerveau à se rappeler les informations que vous avez apprises. C'est une compétence essentielle pour passer le test. C'est aussi une bonne idée de vous chronométrer afin de pouvoir accélérer les problèmes de travail. Essayez de passer des tests d’entraînement et de les terminer dans le même temps que vous aurez en classe.[17]
Facebook
Twitter
Google+
 Minotauromaquia
Minotauromaquia
 1 Recherchez un nombre accru de liaisons sigma pour identifier les réactions d'addition. En d'autres termes, recherchez un plus grand nombre d'atomes que dans la molécule d'origine. Cela se produit généralement en brisant une liaison pi ou en se liant à un ensemble d'électrons non appariés dans la molécule. Les réactions d'addition ne «transforment» pas un atome ou un groupe en un autre. Ils ajoutent simplement quelque chose de nouveau.[1]
1 Recherchez un nombre accru de liaisons sigma pour identifier les réactions d'addition. En d'autres termes, recherchez un plus grand nombre d'atomes que dans la molécule d'origine. Cela se produit généralement en brisant une liaison pi ou en se liant à un ensemble d'électrons non appariés dans la molécule. Les réactions d'addition ne «transforment» pas un atome ou un groupe en un autre. Ils ajoutent simplement quelque chose de nouveau.[1]  2 Recherchez un nombre accru de liaisons pi pour indiquer les réactions d'élimination. C'est le contraire d'une réaction d'addition. Quelque chose sera retiré de la molécule d'origine et laissera des électrons. Ces électrons non liés se présenteront sous la forme d'une paire isolée ou formeront une liaison pi dans la molécule.[2]
2 Recherchez un nombre accru de liaisons pi pour indiquer les réactions d'élimination. C'est le contraire d'une réaction d'addition. Quelque chose sera retiré de la molécule d'origine et laissera des électrons. Ces électrons non liés se présenteront sous la forme d'une paire isolée ou formeront une liaison pi dans la molécule.[2]  3 Notez tout «échange» moléculaire pour isoler les réactions de substitution. Une réaction de substitution se produit lorsqu'un groupe (A) de la molécule est retiré et remplacé par un nouveau groupe (B). Cela ne change pas nécessairement le nombre de liaisons pi ou sigma dans la molécule, comme vous le verrez avec les réactions d’addition et d’élimination. Les types courants de réactions de substitution sont les suivants:[3]
3 Notez tout «échange» moléculaire pour isoler les réactions de substitution. Une réaction de substitution se produit lorsqu'un groupe (A) de la molécule est retiré et remplacé par un nouveau groupe (B). Cela ne change pas nécessairement le nombre de liaisons pi ou sigma dans la molécule, comme vous le verrez avec les réactions d’addition et d’élimination. Les types courants de réactions de substitution sont les suivants:[3]  4 Réactions de réarrangement ponctuel lorsque le produit a la même formule que la molécule d'origine. Les réarrangements forment des isomères - des molécules qui ont exactement les mêmes atomes mais dans une configuration différente. Les isomères auront la même formule chimique, mais des propriétés différentes qui sont uniques à leur configuration. Le nombre de liaisons n'est généralement pas affecté dans les réarrangements.[6]
4 Réactions de réarrangement ponctuel lorsque le produit a la même formule que la molécule d'origine. Les réarrangements forment des isomères - des molécules qui ont exactement les mêmes atomes mais dans une configuration différente. Les isomères auront la même formule chimique, mais des propriétés différentes qui sont uniques à leur configuration. Le nombre de liaisons n'est généralement pas affecté dans les réarrangements.[6]  5 Considérer d'autres réactions importantes qui peuvent affecter les molécules organiques. Les réactions d'oxydo-réduction (ou rédox) sont très courantes en chimie organique, de même que les réactions radicalaires. Vous devriez être un peu familier avec ces réactions de la chimie inorganique générale, mais c'est une bonne idée de les revoir.[7]
5 Considérer d'autres réactions importantes qui peuvent affecter les molécules organiques. Les réactions d'oxydo-réduction (ou rédox) sont très courantes en chimie organique, de même que les réactions radicalaires. Vous devriez être un peu familier avec ces réactions de la chimie inorganique générale, mais c'est une bonne idée de les revoir.[7]  1 Identifier les électrophiles dans les mécanismes de réaction de la chimie organique. Le mot électrophile fait référence aux espèces «aimantes des électrons». Ceci s'applique aux atomes, aux molécules et aux ions. S'il peut accepter une paire d'électrons, il est considéré comme un électrophile. N'oubliez pas que tous les électrophiles n'attirent pas les électrons avec la même intensité. Les électrophiles ayant des électronégativités plus élevées attireront mieux les électrons que ceux ayant des électronégativités plus faibles.[8]
1 Identifier les électrophiles dans les mécanismes de réaction de la chimie organique. Le mot électrophile fait référence aux espèces «aimantes des électrons». Ceci s'applique aux atomes, aux molécules et aux ions. S'il peut accepter une paire d'électrons, il est considéré comme un électrophile. N'oubliez pas que tous les électrophiles n'attirent pas les électrons avec la même intensité. Les électrophiles ayant des électronégativités plus élevées attireront mieux les électrons que ceux ayant des électronégativités plus faibles.[8]  2 Identifier les nucléophiles dans les mécanismes de réaction de la chimie organique. Les nucléophiles sont le complément parfait aux électrophiles. Un nucléophile est une espèce capable de donner une paire d'électrons. Les espèces ayant des électronégativités plus faibles seront plus en mesure de donner des électrons, ce qui les rendra de meilleurs nucléophiles que les espèces ayant des électronégativités plus élevées.[9]
2 Identifier les nucléophiles dans les mécanismes de réaction de la chimie organique. Les nucléophiles sont le complément parfait aux électrophiles. Un nucléophile est une espèce capable de donner une paire d'électrons. Les espèces ayant des électronégativités plus faibles seront plus en mesure de donner des électrons, ce qui les rendra de meilleurs nucléophiles que les espèces ayant des électronégativités plus élevées.[9]  3 Rappelez-vous que les nucléophiles attaquent les électrophiles dans les réactions organiques. Il s’agit, en substance, d’un moyen de considérer les mécanismes de manière cohérente. Vous devriez lire votre mécanisme comme si le composé nucléophile cherche et réagit avec le composé électrophile. Cela vous aidera à vous rappeler par où commencer et où vont les électrons.
3 Rappelez-vous que les nucléophiles attaquent les électrophiles dans les réactions organiques. Il s’agit, en substance, d’un moyen de considérer les mécanismes de manière cohérente. Vous devriez lire votre mécanisme comme si le composé nucléophile cherche et réagit avec le composé électrophile. Cela vous aidera à vous rappeler par où commencer et où vont les électrons.  4 Familiarisez-vous avec d'autres bases de la chimie organique. Bien que la chimie organique soit un sujet important, il existe d’importants principes sous-jacents qui régissent les réactions plus complexes. Si vous vous familiarisez avec ces principes et que vous comprenez leurs applications, vous serez en mesure de voir comment ils se déroulent dans l’ensemble le plus complexe de réactions organiques. Les fondations les plus importantes sont:[10]
4 Familiarisez-vous avec d'autres bases de la chimie organique. Bien que la chimie organique soit un sujet important, il existe d’importants principes sous-jacents qui régissent les réactions plus complexes. Si vous vous familiarisez avec ces principes et que vous comprenez leurs applications, vous serez en mesure de voir comment ils se déroulent dans l’ensemble le plus complexe de réactions organiques. Les fondations les plus importantes sont:[10]  1 Lisez le livre avant de venir en classe. Cela vous permettra de prévisualiser les informations qui seront couvertes dans les conférences. Vous devriez prendre des notes sur ce que vous lisez et assurez-vous qu'elles correspondent aux notes que vous prenez pendant la conférence. Vous devriez également écrire toutes les questions que vous avez pendant la lecture et leur demander si la conférence ne leur répond pas.
1 Lisez le livre avant de venir en classe. Cela vous permettra de prévisualiser les informations qui seront couvertes dans les conférences. Vous devriez prendre des notes sur ce que vous lisez et assurez-vous qu'elles correspondent aux notes que vous prenez pendant la conférence. Vous devriez également écrire toutes les questions que vous avez pendant la lecture et leur demander si la conférence ne leur répond pas.  2 Faites des fiches pour différentes réactions organiques. Vous bénéficierez grandement en divisant les grandes quantités d’informations couvertes dans une classe de chimie organique par des fiches. Le système que vous utilisez pour vos notecards dépendra des informations que vous souhaitez apprendre à ce moment-là. Ne jetez pas vos cartes de correspondance. Gardez-les à revoir chaque semaine, et vous serez beaucoup mieux pour l'examen final.[14]
2 Faites des fiches pour différentes réactions organiques. Vous bénéficierez grandement en divisant les grandes quantités d’informations couvertes dans une classe de chimie organique par des fiches. Le système que vous utilisez pour vos notecards dépendra des informations que vous souhaitez apprendre à ce moment-là. Ne jetez pas vos cartes de correspondance. Gardez-les à revoir chaque semaine, et vous serez beaucoup mieux pour l'examen final.[14]  3 Étudier la chimie organique tous les jours du semestre. Les recherches démontrent que l’incorporation de toutes vos études dans une seule et même session n’est pas très efficace. Vous apprendrez beaucoup plus si vous répartissez votre temps d'étude. N'oubliez pas de prendre une pause d'étude toutes les quarante-cinq minutes pour reposer votre cerveau.[15]
3 Étudier la chimie organique tous les jours du semestre. Les recherches démontrent que l’incorporation de toutes vos études dans une seule et même session n’est pas très efficace. Vous apprendrez beaucoup plus si vous répartissez votre temps d'étude. N'oubliez pas de prendre une pause d'étude toutes les quarante-cinq minutes pour reposer votre cerveau.[15]  4 Passez du temps à étudier en groupe. Même si vous préférez étudier seul, vous découvrirez différentes manières d’examiner les réactions organiques. D'autres étudiants pourraient être efficaces pour déterminer quelles réactions sont SN1 ou SN2, alors que vous êtes mieux en mesure d'identifier les nucléophiles et les électrophiles. Cet échange de connaissances profitera à tous.[16]
4 Passez du temps à étudier en groupe. Même si vous préférez étudier seul, vous découvrirez différentes manières d’examiner les réactions organiques. D'autres étudiants pourraient être efficaces pour déterminer quelles réactions sont SN1 ou SN2, alors que vous êtes mieux en mesure d'identifier les nucléophiles et les électrophiles. Cet échange de connaissances profitera à tous.[16]  5 Prenez au sérieux les problèmes de pratique. Travailler à travers des problèmes de pratique forcera votre cerveau à se rappeler les informations que vous avez apprises. C'est une compétence essentielle pour passer le test. C'est aussi une bonne idée de vous chronométrer afin de pouvoir accélérer les problèmes de travail. Essayez de passer des tests d’entraînement et de les terminer dans le même temps que vous aurez en classe.[17]
5 Prenez au sérieux les problèmes de pratique. Travailler à travers des problèmes de pratique forcera votre cerveau à se rappeler les informations que vous avez apprises. C'est une compétence essentielle pour passer le test. C'est aussi une bonne idée de vous chronométrer afin de pouvoir accélérer les problèmes de travail. Essayez de passer des tests d’entraînement et de les terminer dans le même temps que vous aurez en classe.[17]