La chimie organique a une mauvaise réputation - il n'est pas rare que les étudiants entendent des histoires d'horreur sur la difficulté de la classe avant d'avoir la chance de la prendre eux-mêmes. Bien que la classe puisse être difficile, "O Chem" n'est pas le cauchemar qu'il est souvent censé être. Il y a moins d'informations à mémoriser, mais plus de processus à comprendre. Par conséquent, une compréhension des principes fondamentaux et un bon schéma d'étude sont essentiels pour obtenir une note de passage.
Première partie de trois:
Connaissances de base en chimie
-
 1 Apprenez la définition de "chimie organique"."D'une manière générale, la chimie organique est l'étude de composés chimiques à base de carbone.[1] Le carbone est le sixième élément du tableau périodique et l’un des éléments fondamentaux de la vie sur terre. Les êtres vivants sont constitués de molécules constituées principalement de carbone. Cela signifie que O chem inclut la chimie qui se passe dans votre corps tous les jours. Il comprend également la chimie qui se produit à l'intérieur des animaux, des plantes et des écosystèmes naturels.
1 Apprenez la définition de "chimie organique"."D'une manière générale, la chimie organique est l'étude de composés chimiques à base de carbone.[1] Le carbone est le sixième élément du tableau périodique et l’un des éléments fondamentaux de la vie sur terre. Les êtres vivants sont constitués de molécules constituées principalement de carbone. Cela signifie que O chem inclut la chimie qui se passe dans votre corps tous les jours. Il comprend également la chimie qui se produit à l'intérieur des animaux, des plantes et des écosystèmes naturels. - Cependant, la chimie organique ne se limite pas aux êtres vivants. Par exemple, les réactions chimiques impliquées dans la combustion des combustibles fossiles relèvent de la responsabilité de O Chem parce que ces réactions impliquent des composés à base de carbone dans les combustibles.
-
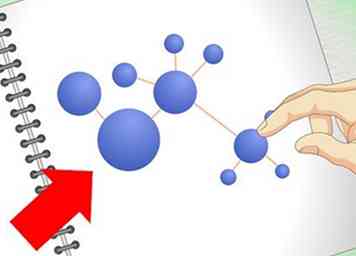 2 Apprenez les moyens courants de représenter des molécules. O chim est un domaine d'étude plus "visuel" que la chimie générale. Vous utiliserez des dessins de molécules et de composés plus souvent que dans les cours de chimie précédents. Savoir interpréter ces sortes de représentations visuelles est l'une des compétences les plus élémentaires et les plus importantes en chimie.
2 Apprenez les moyens courants de représenter des molécules. O chim est un domaine d'étude plus "visuel" que la chimie générale. Vous utiliserez des dessins de molécules et de composés plus souvent que dans les cours de chimie précédents. Savoir interpréter ces sortes de représentations visuelles est l'une des compétences les plus élémentaires et les plus importantes en chimie. - Vous devez vous familiariser avec les structures de Lewis avant de commencer. Ceux-ci sont généralement enseignés dans le cadre d'un cours de chimie générale. Dans une structure de Lewis, les atomes dans une molécule sont représentés par leur symbole chimique (leurs lettres sur le tableau périodique). Les lignes représentent les liens entre elles et les points représentent leurs électrons de valence. Voir notre article sur la structure de Lewis pour un rappel.
- Une façon de dessiner des molécules qui seront probablement nouvelles pour vous est la formule squelettique méthode. Dans une formule squelettique (également appelée "structure de liaison"), les atomes de carbone ne sont pas représentés. Au lieu de cela, il y a juste une ligne pour représenter la liaison. Comme il y a tellement d'atomes de carbone dans O chem, cela rend beaucoup plus rapide pour dessiner des molécules. Les atomes non carbonés sont toujours représentés par leurs symboles chimiques. Un bon guide pour les formations squelettiques est disponible ici.[2]
-
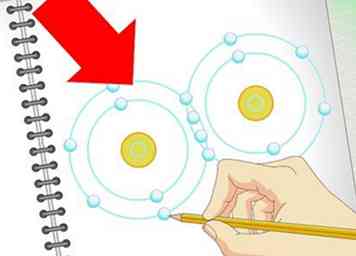 3 Apprenez à représenter les obligations. Covalent les obligations sont de loin le type d'obligations le plus courant en O chimie (bien que la connaissance des liaisons ioniques, etc. soit encore valable). Dans une liaison covalente, deux atomes partagent des électrons non appariés pour former une liaison. Si des électrons non appariés supplémentaires sont disponibles, des atomes à double ou triple liaison sont possibles.
3 Apprenez à représenter les obligations. Covalent les obligations sont de loin le type d'obligations le plus courant en O chimie (bien que la connaissance des liaisons ioniques, etc. soit encore valable). Dans une liaison covalente, deux atomes partagent des électrons non appariés pour former une liaison. Si des électrons non appariés supplémentaires sont disponibles, des atomes à double ou triple liaison sont possibles. - Dans les deux structures de Lewis et les formules squelettiques, les liaisons simples sont représentées par une ligne, les lignes doubles par une ligne double et les liaisons triples par une ligne triple.
- Dans les formules squelettiques, les liaisons entre les atomes de carbone (C) et d’hydrogène (H) ne sont généralement pas dessinées car elles sont si courantes.
- Sauf dans des circonstances particulières, les atomes ne peuvent généralement avoir que huit électrons de valence (enveloppe externe). Cela signifie que la plupart du temps, un atome peut se lier à un maximum de quatre autres atomes.
-
 4 Apprenez les bases de la structure moléculaire 3-D. La chimie organique exige que les élèves réfléchissent aux molécules chimiques réellement exister dans la vie réelle - pas seulement la façon dont ils sont dessinés. Les molécules prennent la forme de structures tridimensionnelles. La nature des liaisons dans la molécule est la chose la plus importante pour déterminer la forme tridimensionnelle d'une molécule, bien que d'autres facteurs puissent parfois jouer un rôle. Voici quelques points à retenir en ce qui concerne la forme des molécules à base de carbone:
4 Apprenez les bases de la structure moléculaire 3-D. La chimie organique exige que les élèves réfléchissent aux molécules chimiques réellement exister dans la vie réelle - pas seulement la façon dont ils sont dessinés. Les molécules prennent la forme de structures tridimensionnelles. La nature des liaisons dans la molécule est la chose la plus importante pour déterminer la forme tridimensionnelle d'une molécule, bien que d'autres facteurs puissent parfois jouer un rôle. Voici quelques points à retenir en ce qui concerne la forme des molécules à base de carbone: - Un carbone lié à quatre autres atomes avec des liaisons simples aura la forme d'un tétraèdre (pyramide à quatre pointes). Un bon exemple est la molécule de méthane (CH4)
- Un carbone lié à un autre atome avec une double liaison et deux atomes avec des liaisons simples a un trigonale plane (triangle plat) forme. L'ion CO3-2 est un bon exemple ici.
- Un carbone lié à deux atomes avec des doubles liaisons ou lié à un album avec une triple liaison a un linéaire (ligne rigide) forme. La molécule de dioxyde de carbone (CO2) en est un exemple.
-
 5 Apprenez à déchiffrer l'hybridation orbitale. Ce sujet a un nom intimidant, mais ce n'est pas cette difficile à comprendre. Essentiellement, orbitales hybrides sont simplement des moyens par lesquels les chimistes représentent les électrons de valence d'un atome en fonction du comportement de cet atome (plutôt que de la manière dont il est dessiné). Si un atome a un certain nombre d'électrons non appariés disponibles pour la liaison mais tend à former un nombre différent de liaisons, il est dit qu'il possède des "orbitales hybrides" pour compenser la différence.
5 Apprenez à déchiffrer l'hybridation orbitale. Ce sujet a un nom intimidant, mais ce n'est pas cette difficile à comprendre. Essentiellement, orbitales hybrides sont simplement des moyens par lesquels les chimistes représentent les électrons de valence d'un atome en fonction du comportement de cet atome (plutôt que de la manière dont il est dessiné). Si un atome a un certain nombre d'électrons non appariés disponibles pour la liaison mais tend à former un nombre différent de liaisons, il est dit qu'il possède des "orbitales hybrides" pour compenser la différence. - Le carbone en est un exemple parfait. Les atomes de carbone ont quatre électrons de valence: deux dans l'orbitale 2 et deux dans l'orbitale 2p. Comme il y a deux électrons non appariés, on peut s'attendre à ce que le carbone forme deux liaisons. Cependant, les expériences montrent que les électrons appariés dans les orbitales 2s forment des liaisons même s'ils ne sont pas appariés. Ainsi, nous disons que l’atome de carbone a quatre électrons non appariés dans une orbitale hybride sp.
-
 6 Apprenez les bases de l'électronégativité. Il y a beaucoup, beaucoup de facteurs qui peuvent déterminer comment deux molécules réagissent entre elles dans O chim. Cependant, l'électronégativité est souvent l'un des facteurs les plus importants. L'électronégativité est un moyen de mesurer la manière dont un atome donné retient ses électrons. Les atomes à haute électronégativité ont tendance à maintenir leurs électrons étroitement (et vice versa pour les atomes à faible électronégativité). Voir notre article sur l'électronégativité pour des informations détaillées.
6 Apprenez les bases de l'électronégativité. Il y a beaucoup, beaucoup de facteurs qui peuvent déterminer comment deux molécules réagissent entre elles dans O chim. Cependant, l'électronégativité est souvent l'un des facteurs les plus importants. L'électronégativité est un moyen de mesurer la manière dont un atome donné retient ses électrons. Les atomes à haute électronégativité ont tendance à maintenir leurs électrons étroitement (et vice versa pour les atomes à faible électronégativité). Voir notre article sur l'électronégativité pour des informations détaillées. - Comme vous allez en haut et à droite dans le tableau périodique, les atomes gagnent plus d'électronégativité (l'hydrogène et l'hélium ne sont pas inclus). Le fluor, l'atome situé tout en haut à droite, a la plus haute électronégativité de tous.
- Parce que les atomes électronégatifs "veulent" plus d'électrons, ils ont tendance à réagir en "attrapant" les électrons disponibles sur d'autres molécules. Par exemple, les atomes comme le chlore et le fluor apparaissent souvent comme des ions négatifs car ils ont pris des électrons d'autres atomes.[3]
Deuxième partie de trois:
Conseils d'étude
-
 1 Ne soyez pas intimidé. La chimie organique introduit beaucoup de nouveaux concepts et vous oblige à réfléchir aux problèmes de chimie de manière nouvelle. Vous devrez apprendre un tout nouveau vocabulaire de chimie. Détendez-vous - tout le monde dans votre classe fait face aux mêmes défis. Etudiez diligemment et obtenez l'aide dont vous avez besoin et vous vous en sortirez probablement bien.
1 Ne soyez pas intimidé. La chimie organique introduit beaucoup de nouveaux concepts et vous oblige à réfléchir aux problèmes de chimie de manière nouvelle. Vous devrez apprendre un tout nouveau vocabulaire de chimie. Détendez-vous - tout le monde dans votre classe fait face aux mêmes défis. Etudiez diligemment et obtenez l'aide dont vous avez besoin et vous vous en sortirez probablement bien. - Ne laissez pas les histoires d'horreur des personnes qui ont pris O chim avant de vous rejoindre. Les étudiants ont tendance à embellir la difficulté de leurs expériences. Entrer dans votre premier test terrifié à l'idée que vous soyez confronté à un défi impossible ne fera que rendre les choses plus difficiles.[4] Au lieu de cela, augmentez votre confiance en passant beaucoup de temps à étudier et à vous reposer la nuit précédente.
-
 2 Concentrez-vous sur la compréhension plutôt que sur la mémorisation. Vous verrez probablement des centaines de réactions différentes dans votre classe O chim. Il est pratiquement impossible de les mémoriser tous, alors ne perdez pas votre temps à les mémoriser mais les plus importants. Au lieu de cela, concentrez-vous sur le principes de base derrière les réactions les plus courantes. La plupart des réactions suivent l'un des quelques schémas, alors bien comprendre ces schémas et savoir comment les appliquer est un moyen beaucoup plus efficace de résoudre correctement les problèmes.
2 Concentrez-vous sur la compréhension plutôt que sur la mémorisation. Vous verrez probablement des centaines de réactions différentes dans votre classe O chim. Il est pratiquement impossible de les mémoriser tous, alors ne perdez pas votre temps à les mémoriser mais les plus importants. Au lieu de cela, concentrez-vous sur le principes de base derrière les réactions les plus courantes. La plupart des réactions suivent l'un des quelques schémas, alors bien comprendre ces schémas et savoir comment les appliquer est un moyen beaucoup plus efficace de résoudre correctement les problèmes. - Cependant, si vous êtes bon en mémorisation, vous pouvez toujours l'utiliser à votre avantage. Essayez d'écrire des mécanismes de réaction de base sur des cartes mémoire et utilisez-les pour mémoriser les réactions. Vous devrez toujours être capable d'ajuster vos connaissances lorsque vous voyez des réactions que vous ne connaissez pas, mais vous pouvez utiliser les principes de base pour vous guider vers le bon mécanisme.
-
 3 Connaissez vos groupes fonctionnels. Basic O chem utilise le même ensemble de structures réactives dans presque toutes ses molécules. Ces structures sont appelées "groupes fonctionnels". Savoir comment identifier ces groupes fonctionnels et comment ils ont tendance à réagir de manière cruciale pour de nombreuses missions O Chem. Étant donné que les groupes fonctionnels réagissent généralement de la même manière avec la cohérence, la connaissance de leurs caractéristiques vous permet de résoudre une grande variété de problèmes.
3 Connaissez vos groupes fonctionnels. Basic O chem utilise le même ensemble de structures réactives dans presque toutes ses molécules. Ces structures sont appelées "groupes fonctionnels". Savoir comment identifier ces groupes fonctionnels et comment ils ont tendance à réagir de manière cruciale pour de nombreuses missions O Chem. Étant donné que les groupes fonctionnels réagissent généralement de la même manière avec la cohérence, la connaissance de leurs caractéristiques vous permet de résoudre une grande variété de problèmes. - Il y a trop de groupes fonctionnels en chimie organique à énumérer dans cet article. Cependant, il n'est pas difficile de trouver des guides sur les groupes fonctionnels en ligne. Par exemple, un bon guide de l'Université Purdue est disponible ici.
-
 4 En cas de doute, suivez le flux d'électrons. À leur niveau le plus élémentaire, la plupart des réactions de chimie organique impliquent seulement l'échange de deux électrons entre plusieurs molécules. Si vous ne parvenez pas à comprendre comment démarrer un mécanisme de réaction, commencez par chercher des endroits où les électrons peuvent transférer. En d'autres termes, recherchez des atomes qui semblent particulièrement bons accepteurs d'électrons et des atomes qui ressemblent particulièrement à de bons donneurs d'électrons. Effectuez le transfert puis demandez: "Que dois-je faire maintenant pour que mes nouvelles molécules atteignent un état stable?"
4 En cas de doute, suivez le flux d'électrons. À leur niveau le plus élémentaire, la plupart des réactions de chimie organique impliquent seulement l'échange de deux électrons entre plusieurs molécules. Si vous ne parvenez pas à comprendre comment démarrer un mécanisme de réaction, commencez par chercher des endroits où les électrons peuvent transférer. En d'autres termes, recherchez des atomes qui semblent particulièrement bons accepteurs d'électrons et des atomes qui ressemblent particulièrement à de bons donneurs d'électrons. Effectuez le transfert puis demandez: "Que dois-je faire maintenant pour que mes nouvelles molécules atteignent un état stable?" - À titre d'exemple, l'oxygène (O) étant plus électronégatif que le carbone, le O lié à C dans un groupe cétone tend à maintenir les électrons de la liaison plus près de lui-même. Cela donne à C une charge partiellement positive et en fait un bon candidat pour recevoir des électrons. Si vous avez un bon donneur d'électrons impliqué dans la réaction, il est logique qu'il puisse attaquer le C, en formant une nouvelle liaison et en déclenchant votre réaction.
-
 5 Utilisez des groupes d'étude pour les devoirs et les tests. Ne vous sentez jamais besoin de vous attaquer à la chimie organique. Se réunir pour faire votre travail avec vos collègues est une idée fantastique. Non seulement les autres peuvent vous aider avec des concepts avec lesquels vous avez des difficultés, mais vous pouvez également acquérir une meilleure compréhension du matériel que vous connaissez déjà en l'expliquant à quelqu'un d'autre.
5 Utilisez des groupes d'étude pour les devoirs et les tests. Ne vous sentez jamais besoin de vous attaquer à la chimie organique. Se réunir pour faire votre travail avec vos collègues est une idée fantastique. Non seulement les autres peuvent vous aider avec des concepts avec lesquels vous avez des difficultés, mais vous pouvez également acquérir une meilleure compréhension du matériel que vous connaissez déjà en l'expliquant à quelqu'un d'autre.
Troisième partie de trois:
Obtenir de l'aide
-
 1 Apprenez à connaître votre professeur. La personne ayant la meilleure connaissance de O chim dans votre classe est la personne qui enseigne la classe. Profitez de cette ressource précieuse. Visitez le bureau de votre professeur pour discuter des domaines avec lesquels vous avez des problèmes. Essayez d'avoir quelques questions claires et succinctes à poser ou un problème avec lequel vous avez des problèmes. Soyez prêt à expliquer le processus de réflexion qui vous a amené à la mauvaise réponse.
1 Apprenez à connaître votre professeur. La personne ayant la meilleure connaissance de O chim dans votre classe est la personne qui enseigne la classe. Profitez de cette ressource précieuse. Visitez le bureau de votre professeur pour discuter des domaines avec lesquels vous avez des problèmes. Essayez d'avoir quelques questions claires et succinctes à poser ou un problème avec lequel vous avez des problèmes. Soyez prêt à expliquer le processus de réflexion qui vous a amené à la mauvaise réponse. - Évitez de marcher dans le bureau de votre professeur sans avoir une idée claire de ce que vous voulez. Le simple fait de dire "Je ne prends pas mes devoirs" ne vous apportera aucune aide utile.
- Non seulement c'est une excellente façon de répondre à vos questions, mais cela peut aussi vous aider à mieux connaître votre professeur. Gardez à l'esprit que si vous visez des études supérieures, vous aurez besoin de quelques références académiques à l'avenir. Les professeurs sont beaucoup plus susceptibles d'écrire de manière positive sur les personnes qui ont pris le temps de leur parler.
-
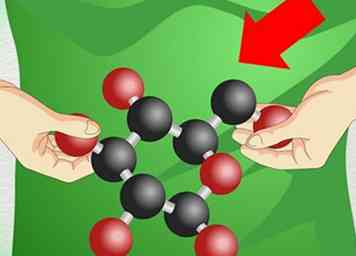 2 Utilisez des outils pour visualiser les problèmes. En chimie, les formes des molécules peuvent déterminer leur réaction. Étant donné qu'il peut être difficile de représenter des molécules 3D complexes sur un morceau de papier plat, l'utilisation de blocs de construction physiques est un excellent moyen de se concentrer sur les structures difficiles.
2 Utilisez des outils pour visualiser les problèmes. En chimie, les formes des molécules peuvent déterminer leur réaction. Étant donné qu'il peut être difficile de représenter des molécules 3D complexes sur un morceau de papier plat, l'utilisation de blocs de construction physiques est un excellent moyen de se concentrer sur les structures difficiles. - Les ensembles de modèles moléculaires vous permettent de construire des molécules à partir de pièces en plastique. Ceux-ci peuvent être assez coûteux si vous les achetez à la librairie de votre école ou à un fournisseur de produits chimiques, mais certains professeurs les prêtent à des étudiants qui les demandent gratuitement.
- Si vous ne pouvez pas mettre la main sur un «vrai» modèle, essayez d’utiliser des balles en mousse, des marqueurs et des chevilles en bois dans votre magasin d’artisanat local pour trouver une solution de bricolage.
- Divers programmes informatiques (comme celui disponible ici) peuvent également vous aider à modéliser des molécules en trois dimensions.[5]
-
 3 Rejoignez la discussion sur les forums d'aide. Une des garnitures d’argent du niveau de difficulté élevé de O chimie est qu’il existe des beaucoup des étudiants à la recherche d'aide en ligne (ainsi que l'offre). Divers forums de chimie en ligne ont de grandes communautés d'utilisateurs prêts à discuter de sujets organiques difficiles. Essayez de publier un problème avec l'un de ces forums, puis travaillez avec les personnes qui vous répondent pour obtenir l'aide dont vous avez besoin.
3 Rejoignez la discussion sur les forums d'aide. Une des garnitures d’argent du niveau de difficulté élevé de O chimie est qu’il existe des beaucoup des étudiants à la recherche d'aide en ligne (ainsi que l'offre). Divers forums de chimie en ligne ont de grandes communautés d'utilisateurs prêts à discuter de sujets organiques difficiles. Essayez de publier un problème avec l'un de ces forums, puis travaillez avec les personnes qui vous répondent pour obtenir l'aide dont vous avez besoin. - Bien qu'il existe de nombreux forums pour ce genre de problèmes, chemicalforums.com est un bon point de départ.[6]
-
 4 Utilisez les ressources en ligne d'O. Une grande variété de sites peut aider à résoudre des problèmes difficiles. Quelques bonnes ressources sont énumérées ci-dessous:
4 Utilisez les ressources en ligne d'O. Une grande variété de sites peut aider à résoudre des problèmes difficiles. Quelques bonnes ressources sont énumérées ci-dessous: - Khan Academy: organise de nombreuses conférences vidéo sur divers sujets de base.[7]
- Chem Helper: A des liens vers des tests pratiques, des forums d'aide, des mécanismes de réaction, etc. Comprend également l'aide de laboratoire.[8]
- Université de Caroline du Sud Aiken: comprend son propre répertoire de sites Web utiles couvrant une variété de sujets relatifs à la chimie.
Facebook
Twitter
Google+
 Minotauromaquia
Minotauromaquia
 1 Apprenez la définition de "chimie organique"."D'une manière générale, la chimie organique est l'étude de composés chimiques à base de carbone.[1] Le carbone est le sixième élément du tableau périodique et l’un des éléments fondamentaux de la vie sur terre. Les êtres vivants sont constitués de molécules constituées principalement de carbone. Cela signifie que O chem inclut la chimie qui se passe dans votre corps tous les jours. Il comprend également la chimie qui se produit à l'intérieur des animaux, des plantes et des écosystèmes naturels.
1 Apprenez la définition de "chimie organique"."D'une manière générale, la chimie organique est l'étude de composés chimiques à base de carbone.[1] Le carbone est le sixième élément du tableau périodique et l’un des éléments fondamentaux de la vie sur terre. Les êtres vivants sont constitués de molécules constituées principalement de carbone. Cela signifie que O chem inclut la chimie qui se passe dans votre corps tous les jours. Il comprend également la chimie qui se produit à l'intérieur des animaux, des plantes et des écosystèmes naturels.  2 Apprenez les moyens courants de représenter des molécules. O chim est un domaine d'étude plus "visuel" que la chimie générale. Vous utiliserez des dessins de molécules et de composés plus souvent que dans les cours de chimie précédents. Savoir interpréter ces sortes de représentations visuelles est l'une des compétences les plus élémentaires et les plus importantes en chimie.
2 Apprenez les moyens courants de représenter des molécules. O chim est un domaine d'étude plus "visuel" que la chimie générale. Vous utiliserez des dessins de molécules et de composés plus souvent que dans les cours de chimie précédents. Savoir interpréter ces sortes de représentations visuelles est l'une des compétences les plus élémentaires et les plus importantes en chimie.  3 Apprenez à représenter les obligations. Covalent les obligations sont de loin le type d'obligations le plus courant en O chimie (bien que la connaissance des liaisons ioniques, etc. soit encore valable). Dans une liaison covalente, deux atomes partagent des électrons non appariés pour former une liaison. Si des électrons non appariés supplémentaires sont disponibles, des atomes à double ou triple liaison sont possibles.
3 Apprenez à représenter les obligations. Covalent les obligations sont de loin le type d'obligations le plus courant en O chimie (bien que la connaissance des liaisons ioniques, etc. soit encore valable). Dans une liaison covalente, deux atomes partagent des électrons non appariés pour former une liaison. Si des électrons non appariés supplémentaires sont disponibles, des atomes à double ou triple liaison sont possibles.  4 Apprenez les bases de la structure moléculaire 3-D. La chimie organique exige que les élèves réfléchissent aux molécules chimiques réellement exister dans la vie réelle - pas seulement la façon dont ils sont dessinés. Les molécules prennent la forme de structures tridimensionnelles. La nature des liaisons dans la molécule est la chose la plus importante pour déterminer la forme tridimensionnelle d'une molécule, bien que d'autres facteurs puissent parfois jouer un rôle. Voici quelques points à retenir en ce qui concerne la forme des molécules à base de carbone:
4 Apprenez les bases de la structure moléculaire 3-D. La chimie organique exige que les élèves réfléchissent aux molécules chimiques réellement exister dans la vie réelle - pas seulement la façon dont ils sont dessinés. Les molécules prennent la forme de structures tridimensionnelles. La nature des liaisons dans la molécule est la chose la plus importante pour déterminer la forme tridimensionnelle d'une molécule, bien que d'autres facteurs puissent parfois jouer un rôle. Voici quelques points à retenir en ce qui concerne la forme des molécules à base de carbone:  5 Apprenez à déchiffrer l'hybridation orbitale. Ce sujet a un nom intimidant, mais ce n'est pas cette difficile à comprendre. Essentiellement, orbitales hybrides sont simplement des moyens par lesquels les chimistes représentent les électrons de valence d'un atome en fonction du comportement de cet atome (plutôt que de la manière dont il est dessiné). Si un atome a un certain nombre d'électrons non appariés disponibles pour la liaison mais tend à former un nombre différent de liaisons, il est dit qu'il possède des "orbitales hybrides" pour compenser la différence.
5 Apprenez à déchiffrer l'hybridation orbitale. Ce sujet a un nom intimidant, mais ce n'est pas cette difficile à comprendre. Essentiellement, orbitales hybrides sont simplement des moyens par lesquels les chimistes représentent les électrons de valence d'un atome en fonction du comportement de cet atome (plutôt que de la manière dont il est dessiné). Si un atome a un certain nombre d'électrons non appariés disponibles pour la liaison mais tend à former un nombre différent de liaisons, il est dit qu'il possède des "orbitales hybrides" pour compenser la différence.  6 Apprenez les bases de l'électronégativité. Il y a beaucoup, beaucoup de facteurs qui peuvent déterminer comment deux molécules réagissent entre elles dans O chim. Cependant, l'électronégativité est souvent l'un des facteurs les plus importants. L'électronégativité est un moyen de mesurer la manière dont un atome donné retient ses électrons. Les atomes à haute électronégativité ont tendance à maintenir leurs électrons étroitement (et vice versa pour les atomes à faible électronégativité). Voir notre article sur l'électronégativité pour des informations détaillées.
6 Apprenez les bases de l'électronégativité. Il y a beaucoup, beaucoup de facteurs qui peuvent déterminer comment deux molécules réagissent entre elles dans O chim. Cependant, l'électronégativité est souvent l'un des facteurs les plus importants. L'électronégativité est un moyen de mesurer la manière dont un atome donné retient ses électrons. Les atomes à haute électronégativité ont tendance à maintenir leurs électrons étroitement (et vice versa pour les atomes à faible électronégativité). Voir notre article sur l'électronégativité pour des informations détaillées.  1 Ne soyez pas intimidé. La chimie organique introduit beaucoup de nouveaux concepts et vous oblige à réfléchir aux problèmes de chimie de manière nouvelle. Vous devrez apprendre un tout nouveau vocabulaire de chimie. Détendez-vous - tout le monde dans votre classe fait face aux mêmes défis. Etudiez diligemment et obtenez l'aide dont vous avez besoin et vous vous en sortirez probablement bien.
1 Ne soyez pas intimidé. La chimie organique introduit beaucoup de nouveaux concepts et vous oblige à réfléchir aux problèmes de chimie de manière nouvelle. Vous devrez apprendre un tout nouveau vocabulaire de chimie. Détendez-vous - tout le monde dans votre classe fait face aux mêmes défis. Etudiez diligemment et obtenez l'aide dont vous avez besoin et vous vous en sortirez probablement bien.  2 Concentrez-vous sur la compréhension plutôt que sur la mémorisation. Vous verrez probablement des centaines de réactions différentes dans votre classe O chim. Il est pratiquement impossible de les mémoriser tous, alors ne perdez pas votre temps à les mémoriser mais les plus importants. Au lieu de cela, concentrez-vous sur le principes de base derrière les réactions les plus courantes. La plupart des réactions suivent l'un des quelques schémas, alors bien comprendre ces schémas et savoir comment les appliquer est un moyen beaucoup plus efficace de résoudre correctement les problèmes.
2 Concentrez-vous sur la compréhension plutôt que sur la mémorisation. Vous verrez probablement des centaines de réactions différentes dans votre classe O chim. Il est pratiquement impossible de les mémoriser tous, alors ne perdez pas votre temps à les mémoriser mais les plus importants. Au lieu de cela, concentrez-vous sur le principes de base derrière les réactions les plus courantes. La plupart des réactions suivent l'un des quelques schémas, alors bien comprendre ces schémas et savoir comment les appliquer est un moyen beaucoup plus efficace de résoudre correctement les problèmes.  3 Connaissez vos groupes fonctionnels. Basic O chem utilise le même ensemble de structures réactives dans presque toutes ses molécules. Ces structures sont appelées "groupes fonctionnels". Savoir comment identifier ces groupes fonctionnels et comment ils ont tendance à réagir de manière cruciale pour de nombreuses missions O Chem. Étant donné que les groupes fonctionnels réagissent généralement de la même manière avec la cohérence, la connaissance de leurs caractéristiques vous permet de résoudre une grande variété de problèmes.
3 Connaissez vos groupes fonctionnels. Basic O chem utilise le même ensemble de structures réactives dans presque toutes ses molécules. Ces structures sont appelées "groupes fonctionnels". Savoir comment identifier ces groupes fonctionnels et comment ils ont tendance à réagir de manière cruciale pour de nombreuses missions O Chem. Étant donné que les groupes fonctionnels réagissent généralement de la même manière avec la cohérence, la connaissance de leurs caractéristiques vous permet de résoudre une grande variété de problèmes.  4 En cas de doute, suivez le flux d'électrons. À leur niveau le plus élémentaire, la plupart des réactions de chimie organique impliquent seulement l'échange de deux électrons entre plusieurs molécules. Si vous ne parvenez pas à comprendre comment démarrer un mécanisme de réaction, commencez par chercher des endroits où les électrons peuvent transférer. En d'autres termes, recherchez des atomes qui semblent particulièrement bons accepteurs d'électrons et des atomes qui ressemblent particulièrement à de bons donneurs d'électrons. Effectuez le transfert puis demandez: "Que dois-je faire maintenant pour que mes nouvelles molécules atteignent un état stable?"
4 En cas de doute, suivez le flux d'électrons. À leur niveau le plus élémentaire, la plupart des réactions de chimie organique impliquent seulement l'échange de deux électrons entre plusieurs molécules. Si vous ne parvenez pas à comprendre comment démarrer un mécanisme de réaction, commencez par chercher des endroits où les électrons peuvent transférer. En d'autres termes, recherchez des atomes qui semblent particulièrement bons accepteurs d'électrons et des atomes qui ressemblent particulièrement à de bons donneurs d'électrons. Effectuez le transfert puis demandez: "Que dois-je faire maintenant pour que mes nouvelles molécules atteignent un état stable?"  5 Utilisez des groupes d'étude pour les devoirs et les tests. Ne vous sentez jamais besoin de vous attaquer à la chimie organique. Se réunir pour faire votre travail avec vos collègues est une idée fantastique. Non seulement les autres peuvent vous aider avec des concepts avec lesquels vous avez des difficultés, mais vous pouvez également acquérir une meilleure compréhension du matériel que vous connaissez déjà en l'expliquant à quelqu'un d'autre.
5 Utilisez des groupes d'étude pour les devoirs et les tests. Ne vous sentez jamais besoin de vous attaquer à la chimie organique. Se réunir pour faire votre travail avec vos collègues est une idée fantastique. Non seulement les autres peuvent vous aider avec des concepts avec lesquels vous avez des difficultés, mais vous pouvez également acquérir une meilleure compréhension du matériel que vous connaissez déjà en l'expliquant à quelqu'un d'autre.  1 Apprenez à connaître votre professeur. La personne ayant la meilleure connaissance de O chim dans votre classe est la personne qui enseigne la classe. Profitez de cette ressource précieuse. Visitez le bureau de votre professeur pour discuter des domaines avec lesquels vous avez des problèmes. Essayez d'avoir quelques questions claires et succinctes à poser ou un problème avec lequel vous avez des problèmes. Soyez prêt à expliquer le processus de réflexion qui vous a amené à la mauvaise réponse.
1 Apprenez à connaître votre professeur. La personne ayant la meilleure connaissance de O chim dans votre classe est la personne qui enseigne la classe. Profitez de cette ressource précieuse. Visitez le bureau de votre professeur pour discuter des domaines avec lesquels vous avez des problèmes. Essayez d'avoir quelques questions claires et succinctes à poser ou un problème avec lequel vous avez des problèmes. Soyez prêt à expliquer le processus de réflexion qui vous a amené à la mauvaise réponse.  2 Utilisez des outils pour visualiser les problèmes. En chimie, les formes des molécules peuvent déterminer leur réaction. Étant donné qu'il peut être difficile de représenter des molécules 3D complexes sur un morceau de papier plat, l'utilisation de blocs de construction physiques est un excellent moyen de se concentrer sur les structures difficiles.
2 Utilisez des outils pour visualiser les problèmes. En chimie, les formes des molécules peuvent déterminer leur réaction. Étant donné qu'il peut être difficile de représenter des molécules 3D complexes sur un morceau de papier plat, l'utilisation de blocs de construction physiques est un excellent moyen de se concentrer sur les structures difficiles.  3 Rejoignez la discussion sur les forums d'aide. Une des garnitures d’argent du niveau de difficulté élevé de O chimie est qu’il existe des beaucoup des étudiants à la recherche d'aide en ligne (ainsi que l'offre). Divers forums de chimie en ligne ont de grandes communautés d'utilisateurs prêts à discuter de sujets organiques difficiles. Essayez de publier un problème avec l'un de ces forums, puis travaillez avec les personnes qui vous répondent pour obtenir l'aide dont vous avez besoin.
3 Rejoignez la discussion sur les forums d'aide. Une des garnitures d’argent du niveau de difficulté élevé de O chimie est qu’il existe des beaucoup des étudiants à la recherche d'aide en ligne (ainsi que l'offre). Divers forums de chimie en ligne ont de grandes communautés d'utilisateurs prêts à discuter de sujets organiques difficiles. Essayez de publier un problème avec l'un de ces forums, puis travaillez avec les personnes qui vous répondent pour obtenir l'aide dont vous avez besoin.  4 Utilisez les ressources en ligne d'O. Une grande variété de sites peut aider à résoudre des problèmes difficiles. Quelques bonnes ressources sont énumérées ci-dessous:
4 Utilisez les ressources en ligne d'O. Une grande variété de sites peut aider à résoudre des problèmes difficiles. Quelques bonnes ressources sont énumérées ci-dessous: